题目内容
17.在密闭容器里,发生反应2A(g)+B(g)?2C(g),下列不能说明该反应达到化学平衡的是( )| A. | 2v正(B)=v逆(C) | B. | 该体系的密度都不随时间变化 | ||
| C. | 1molA断裂,同时1molC也断裂 | D. | 该体系的温度不随时间而变化 |
分析 可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量、物质的量浓度、百分含量及由此引起的一系列物理量不变,据此分析解答.
解答 解:可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量、物质的量浓度、百分含量及由此引起的一系列物理量不变,
A.2v正(B)=v逆(C)=2v逆(B),B的正逆反应速率相等,该反应达到平衡状态,故A不选;
B.该反应前后混合气体质量不变、容器体积不变,导致密度始终不变,所以该体系的密度都不随时间变化时该反应不一定达到平衡状态,故B选;
C.1molA断裂,反应正向移动,同时1molC也断裂,反应逆向移动同时生成1molA,A的正逆反应速率相等,该反应达到平衡状态,故C不选;
D.该反应的正反应无论是吸热反应还是放热反应,随着反应的进行反应体系温度改变,当该体系的温度不随时间而变化时正逆反应速率相等,该反应达到平衡状态,故D不选;
故选B.
点评 本题考查化学平衡状态判断,为高频考点,明确化学平衡状态判断方法是解本题关键,注意:只有反应前后改变的物理量不变时可逆反应才能达到平衡状态,易错选项是B.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
7.将1体积A(g)和3体积B(g)混合,在5000C和催化剂存在下发生如下反应:2A(g)+B(g)?2C (g)并达到平衡状态,在同温同压下测得此反应在平衡前后的气体密度之比为9/10,此时A的转化率为( )
| A. | 90% | B. | 80% | C. | 45% | D. | 10% |
8.已知稀硝酸和稀硫酸组成的混酸中c(NO3-)+c(SO42-)=5mol•L-1,若取一定量的混酸溶解铜粉达到最大值(假设还原产物只有NO),则混酸中HNO3、H2SO4的物质的量浓度之比为( )
| A. | 1:1 | B. | 3:2 | C. | 2:3 | D. | 2:1 |
5.下列说法正确的是( )
| A. | 18g水含有的原子数为NA | |
| B. | 4g金属钙变成钙离子时失去的电子数为0.1NA | |
| C. | 1molO2的质量等于1mol氧原子的质量 | |
| D. | 24gO2和24gO3所含的原子数目相等 |
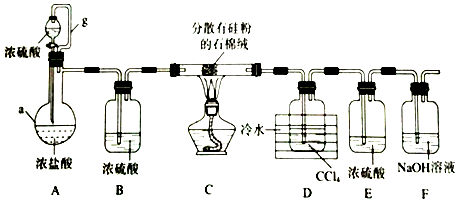
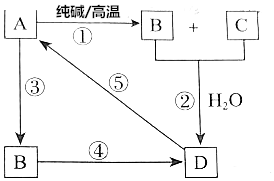 已知A是一种不溶于水的酸酐.根据如图所示转化关系,请完成下列空白.
已知A是一种不溶于水的酸酐.根据如图所示转化关系,请完成下列空白.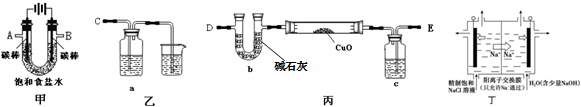
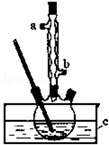 正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小.某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:2C3CH2CH2CH2OH$→_{135°}^{浓H_{2}SO_{4}}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小.某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:2C3CH2CH2CH2OH$→_{135°}^{浓H_{2}SO_{4}}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O