��Ŀ����
 �õ������մɴ���������췢���������Ȳ������ܴ������߷���������Ч�ʣ���ҵ���û�ѧ����������Ʊ������裬�䷴Ӧ���£�3SiCl4��g��+2N2��g��+6H2��g��
�õ������մɴ���������췢���������Ȳ������ܴ������߷���������Ч�ʣ���ҵ���û�ѧ����������Ʊ������裬�䷴Ӧ���£�3SiCl4��g��+2N2��g��+6H2��g��| �� |
��1��SiCl4��ƽ����Ӧ����Ϊ
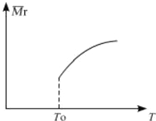
��2��ƽ������ı��¶ȣ���������ƽ����Է����������¶ȵĹ�ϵ��ͼ��ʾ������˵����ȷ����
A���÷�Ӧ���κ��¶��¿��Է�����
B���������������������䣬����������Ӧ���ﵽƽ��״̬
C�������������䣬����Si3N4�����ʵ�����ƽ�������ƶ�
D����3��2��6�����ʵ��������ӷ�Ӧ�SiC14��g����ת���ʽ���
��3���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ��������������ͬʱ����
��T3�����¶��·�Ӧ�ﵽƽ������ʱ�����
| �¶�T | T1 | T2 | T3 |
| ƽ�ⳣ��K | 1.2 | 2.5 | 10 |
x mol/L��c ��HCl��=0.3mol/L������Si3N4 ��s������Ҫʹƽ�⽨���Ĺ�����HClŨ�ȼ�С��x��ȡֵ
��ΧΪ
��4���÷�Ӧ��ԭ��������Ϊ
��5����ҵ���Ʊ�SiCl4�ķ�Ӧ�������£�
��SiO2��s��+2C��s���TSi��s��+2CO��g������H�TakJ/mol
��Si��s��+2Cl2��g���TSiCl4��l������H=bkJ/mol
��SiCl4��g���TSiCl4��l������H�TckJ/mol
д���������衢��̿��Cl 2�ڸ����·�Ӧ������̬SiC14��һ����̼���Ȼ�ѧ����ʽ
���㣺��ѧƽ��ļ���,�Ȼ�ѧ����ʽ,��Ӧ���ʵĶ�����ʾ����,��ѧƽ��״̬���ж�
ר�⣺��ѧƽ��ר��
��������1�����������������2.80gΪSi3N4������������n=
���������ʵ��������ݷ���ʽ��������SiCl4�����ʵ������ٸ���v=
����v��SiCl4����
��2��ƽ��������Ӧ�����ƶ�ʱ�����������������С��������������ʵ�������������ƽ����Է���������С����ͼ��֪�����¶����ߣ������ƽ����Է�����������˵������ʱƽ�������ƶ�������ӦΪ���ȷ�Ӧ��������������ƽ���ƶ�Ӱ�켰����ƽ����������ȡ������������ɴ�������һЩ����������
��3���¶�Խ�ͣ���Ӧ����Խ��������ƽ��ʱ��Խ������Q��K����ֵ�Ƚ��жϷ�Ӧ����
��4��ԭ��������=��Ŀ���������/����ѧ����ʽ������������������100%��
��5��������֪�Ȼ�ѧ����ʽ��˹������д��
| m |
| M |
| ||
| ��t |
��2��ƽ��������Ӧ�����ƶ�ʱ�����������������С��������������ʵ�������������ƽ����Է���������С����ͼ��֪�����¶����ߣ������ƽ����Է�����������˵������ʱƽ�������ƶ�������ӦΪ���ȷ�Ӧ��������������ƽ���ƶ�Ӱ�켰����ƽ����������ȡ������������ɴ�������һЩ����������
��3���¶�Խ�ͣ���Ӧ����Խ��������ƽ��ʱ��Խ������Q��K����ֵ�Ƚ��жϷ�Ӧ����
��4��ԭ��������=��Ŀ���������/����ѧ����ʽ������������������100%��
��5��������֪�Ȼ�ѧ����ʽ��˹������д��
���
�⣺��1�����������������2.80gΪSi3N4�������������ʵ���
=0.02mol�����ݷ���ʽ��֪����SiCl4�����ʵ���=0.02mol��3=0.06mol����v��SiCl4��=
=0.015mol/��L��min����
�ʴ�Ϊ��0.015mol/��L��min����
��2��A����ͼ��֪�����¶����ߣ������ƽ����Է�����������˵������ӦΪ���ȷ�Ӧ������H��0����Ӧ�ġ�S��0����H-T��S��0ʱ��Ӧ�ܹ��Է����У������κ��¶��·�Ӧ���ܹ��Է����У���A��ȷ��
B��Si3N4�ǹ��壬�淴Ӧ���л���������������С���������������������䣬����������Ӧ���ﵽƽ��״̬����B��ȷ��
C��Si3N4�ǹ��壬���������ʵ�������Ӱ��ƽ���ƶ�����C����
D����3��2��6�����ʵ��������ӷ�Ӧ��൱����������Ũ�ȣ�SiC14��g����ת�������ߣ���D����
�ʴ�Ϊ��AB��
��3������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С�����¶�T1��T2��T3���¶�Խ�ͣ���Ӧ����Խ��������ƽ��ʱ��Խ�������¶�T3�ﵽƽ��ʱ�����Q=
��K=1.2ʱ��ƽ�������ƶ���0��x��0.15ʱ���ϣ��ʴ�Ϊ��T3��0��x��0.15��
��4��ԭ��������=��Ŀ���������/����ѧ����ʽ������������������100%���ʸ÷�Ӧԭ��������=[��28��3+14��4���£�28��3+14��4+36.6��12��]��100%=24.22%��
�ʴ�Ϊ��24.22%��
��5����֪
��SiO2��s��+2C��s���TSi��s��+2CO��g������H�TakJ/mol
��Si��s��+2Cl2��g���TSiCl4��l������H=bkJ/mol
��SiCl4��g���TSiCl4��l������H�TckJ/mol
�ݸ�˹���ɣ���+��-�۵ã�SiO2��s��+2C��s��+2Cl2��g���TSiCl4��g��+2CO��g����=��a+b-c��KJ/mol���ʴ�Ϊ��SiO2��s��+2C��s��+2Cl2��g���TSiCl4��g��+2CO��g����=��a+b-c��KJ/mol��
| 2.8g |
| 140g/mol |
| ||
| 2min |
�ʴ�Ϊ��0.015mol/��L��min����
��2��A����ͼ��֪�����¶����ߣ������ƽ����Է�����������˵������ӦΪ���ȷ�Ӧ������H��0����Ӧ�ġ�S��0����H-T��S��0ʱ��Ӧ�ܹ��Է����У������κ��¶��·�Ӧ���ܹ��Է����У���A��ȷ��
B��Si3N4�ǹ��壬�淴Ӧ���л���������������С���������������������䣬����������Ӧ���ﵽƽ��״̬����B��ȷ��
C��Si3N4�ǹ��壬���������ʵ�������Ӱ��ƽ���ƶ�����C����
D����3��2��6�����ʵ��������ӷ�Ӧ��൱����������Ũ�ȣ�SiC14��g����ת�������ߣ���D����
�ʴ�Ϊ��AB��
��3������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С�����¶�T1��T2��T3���¶�Խ�ͣ���Ӧ����Խ��������ƽ��ʱ��Խ�������¶�T3�ﵽƽ��ʱ�����Q=
| [HCl]12 |
| [SiCl]3?[N2]2?[H2]6 |
��4��ԭ��������=��Ŀ���������/����ѧ����ʽ������������������100%���ʸ÷�Ӧԭ��������=[��28��3+14��4���£�28��3+14��4+36.6��12��]��100%=24.22%��
�ʴ�Ϊ��24.22%��
��5����֪
��SiO2��s��+2C��s���TSi��s��+2CO��g������H�TakJ/mol
��Si��s��+2Cl2��g���TSiCl4��l������H=bkJ/mol
��SiCl4��g���TSiCl4��l������H�TckJ/mol
�ݸ�˹���ɣ���+��-�۵ã�SiO2��s��+2C��s��+2Cl2��g���TSiCl4��g��+2CO��g����=��a+b-c��KJ/mol���ʴ�Ϊ��SiO2��s��+2C��s��+2Cl2��g���TSiCl4��g��+2CO��g����=��a+b-c��KJ/mol��
���������⿼�黯ѧ��Ӧ���ʼ��㡢���������ƽ���ƶ�Ӱ�졢ƽ�ⳣ��Ӱ�����ء�ԭ�������ʵļ���ȣ���Ŀ�Ѷ��еȣ�ע�ضԳ���֪ʶ��Ŀ��飬�ܽϺõ�����ѧ��������������������

��ϰ��ϵ�д�
 ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
�����Ŀ
���б仯�У����ڷ��ȷ�Ӧ���ǣ�������
| A��H2O��g���TH2O��l����H=-44kJ/mol |
| B��2HI��g���TH2��g��+I2��g����H=+14.9kJ/mol |
C��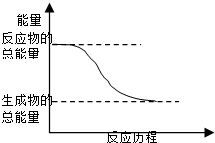 �����仯��ͼ��ʾ�Ļ�ѧ��Ӧ |
| D���γɻ�ѧ��ʱ�ų������Ļ�ѧ��Ӧ |

 ��1��ij��ʯ�ɼ��ֳ�����������ɣ������Щ�������Ԫ���ڵؿ��еĺ������ܷḻ����ÿ�ʯ��Ϸ�ĩ�м������������������Һ�����˵ÿ�������ɫͿ�ϵĺ���ɫ�������ɫ��Һ��Ȼ����������Һ�е������ᣬ���ó������������������������Ĺ�ϵ��ͼ��ʾ��
��1��ij��ʯ�ɼ��ֳ�����������ɣ������Щ�������Ԫ���ڵؿ��еĺ������ܷḻ����ÿ�ʯ��Ϸ�ĩ�м������������������Һ�����˵ÿ�������ɫͿ�ϵĺ���ɫ�������ɫ��Һ��Ȼ����������Һ�е������ᣬ���ó������������������������Ĺ�ϵ��ͼ��ʾ�� �������IJ�ҵ���������ɡ���������ȡ������ұ�������ļӹ��Ȼ��ڹ��ɣ���ش��������⣺
�������IJ�ҵ���������ɡ���������ȡ������ұ�������ļӹ��Ȼ��ڹ��ɣ���ش��������⣺