题目内容
X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大,Z基态原子核外有三个未成对电子,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V形,Q的各级电离能如下表,W与R是同族元素.
回答下列有关问题:
(1)W原子的价电子排布图为 .
(2)化合物Q2W2的电子式 ,化合物XYZ的结构式 .
(3)Y、Z、W分别与X形成常见化合物的沸点由高到低的顺序是 (用分子式表示).
(4)RW3分子的立体构型为 ,键角为 .
(5)根据等电子原理,指出与YW2互为等电子体且含有Z原子的微粒有 、 (要求写一种分子和一种离子).
(6)Y的一种氢化物相对分子质量为28,其中分子中的σ键与π键的键数之比为 ,该氢化物与氧气形成的燃料电池在碱性电解质中正极反应式为 .
| Q | I1 | I2 | I3 | I4 | I5 | … |
| 电离能(kJ/mol) | 496 | 4562 | 6912 | 9543 | 13353 | … |
(1)W原子的价电子排布图为
(2)化合物Q2W2的电子式
(3)Y、Z、W分别与X形成常见化合物的沸点由高到低的顺序是
(4)RW3分子的立体构型为
(5)根据等电子原理,指出与YW2互为等电子体且含有Z原子的微粒有
(6)Y的一种氢化物相对分子质量为28,其中分子中的σ键与π键的键数之比为
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大,Z基态原子核外有三个未成对电子,则Z为第ⅤA族元素,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V形,则X为氢元素,Y为碳元素,Z为氮元素,W为氧元素,根据Q的各级电离能可知,Q最外层有1个电子,则Q为钠元素,W与R是同族元素,则R为硫元素,据此答题;
解答:
解:X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大,Z基态原子核外有三个未成对电子,则Z为第ⅤA族元素,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V形,则X为氢元素,Y为碳元素,Z为氮元素,W为氧元素,根据Q的各级电离能可知,Q最外层有1个电子,则Q为钠元素,W与R是同族元素,则R为硫元素,
(1)W为氧元素,原子的价电子排布图为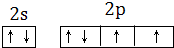 ,
,
故答案为: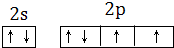 ;
;
(2)化合物Q2W2为过氧化钠,它的电子式为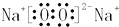 ,化合物XYZ的结构式为H-C≡N,
,化合物XYZ的结构式为H-C≡N,
故答案为: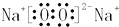 ;H-C≡N;
;H-C≡N;
(3)Y、Z、W分别与X形成常见化合物分别为CH4、NH3、H2O,它们的沸点由高到低的顺序是H2O>NH3>CH4,
故答案为:H2O>NH3>CH4;
(4)SO3分子中,S原子的价层电子对数为
=3,没有孤电子对,所以分子的立体构型为平面三角形,键角为120°,
故答案为:平面三角形;120°;
(5)与二氧化碳为等电子体的微粒有N2O; SCN- (或OCN-、N3-、NO2+)等,
故答案为:N2O; SCN- (或OCN-、N3-、NO2+)等;
出与YW2互为等电子体且含有Z原子的微粒有、(要求写一种分子和一种离子).
(6)Y的一种氢化物相对分子质量为28,该物质为C2H4,分子中有5σ个与1个π键,所以σ键与π键的键数之比为5:1,乙烯与氧气形成的燃料电池在碱性电解质中,氧气做氧化剂,在正极发生还原反应,电极反应式为 O2+4e-+2H2O=4OH-,
故答案为:5:1;O2+4e-+2H2O=4OH-;
(1)W为氧元素,原子的价电子排布图为
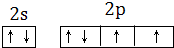 ,
,故答案为:
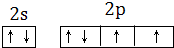 ;
; (2)化合物Q2W2为过氧化钠,它的电子式为
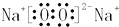 ,化合物XYZ的结构式为H-C≡N,
,化合物XYZ的结构式为H-C≡N,故答案为:
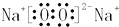 ;H-C≡N;
;H-C≡N;(3)Y、Z、W分别与X形成常见化合物分别为CH4、NH3、H2O,它们的沸点由高到低的顺序是H2O>NH3>CH4,
故答案为:H2O>NH3>CH4;
(4)SO3分子中,S原子的价层电子对数为
| 6+0 |
| 2 |
故答案为:平面三角形;120°;
(5)与二氧化碳为等电子体的微粒有N2O; SCN- (或OCN-、N3-、NO2+)等,
故答案为:N2O; SCN- (或OCN-、N3-、NO2+)等;
出与YW2互为等电子体且含有Z原子的微粒有、(要求写一种分子和一种离子).
(6)Y的一种氢化物相对分子质量为28,该物质为C2H4,分子中有5σ个与1个π键,所以σ键与π键的键数之比为5:1,乙烯与氧气形成的燃料电池在碱性电解质中,氧气做氧化剂,在正极发生还原反应,电极反应式为 O2+4e-+2H2O=4OH-,
故答案为:5:1;O2+4e-+2H2O=4OH-;
点评:本题主要考查了电子排布式、电子式、结构式、分子空间构型、等电子体、原电池电极反应等知识点,中等难度,涉及知识点较多,元素推断是解题的关键,答题时注意化学用语的正确表达.

练习册系列答案
相关题目
水是生命之源、生态之基,下列关于水的描述正确的是( )
| A、H216O中,质量数之和是质子数之和的两倍 |
| B、在纯水中加入少量铵盐不会对水的电离产生影响 |
| C、100℃时,纯水的pH=7 |
D、H2O的电子式为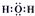 |
实验室需配制一种仅含五种离子(水电离出的离子可忽略)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为1mol/L,下面四个选项中能达到此目的是( )
| A、Ca2+、K+、OH-、Cl-、NO3- |
| B、Fe2+、H+、Br+、NO3-、Cl- |
| C、Na+、NH4+、SO42-、NO3-、Cl- |
| D、Al3+、H+、Cl-、SO42-、NO3- |


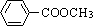 、
、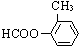 、
、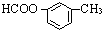 、
、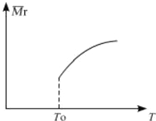 用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g)
用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g)
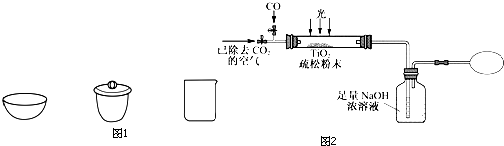
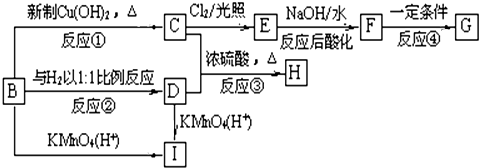
 阅读下列实验内容,根据题目要求回答问题.
阅读下列实验内容,根据题目要求回答问题.