题目内容
下列表示方法错误的是( )
A、氮分子的电子式: |
B、Cl-的离子结构示意图: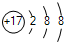 |
C、甲烷分子的比例模型: |
D、乙烯分子的球棍模型: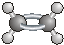 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氮气分子的电子式中,漏掉的氮原子的最外层1对孤电子对;
B.氯离子的核电荷数为17,核外电子总数为18,最外层达到8电子稳定结构;
C.甲烷为正四面体结构,碳原子半径大于大于氢原子;
D.乙烯分子中中存在碳碳双键,所有原子共平面.
B.氯离子的核电荷数为17,核外电子总数为18,最外层达到8电子稳定结构;
C.甲烷为正四面体结构,碳原子半径大于大于氢原子;
D.乙烯分子中中存在碳碳双键,所有原子共平面.
解答:
解:A.氮气分子中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气的电子式为: ,故A错误;
,故A错误;
B.氯离子核电荷数为17,最外层达到8电子稳定结构,Cl-的离子结构示意图为: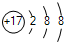 ,故B正确;
,故B正确;
C.甲烷分子中存在4个碳氢键,为正四面体结构,碳原子半径大于氢原子,甲烷的球棍模型为: ,故C正确;
,故C正确;
D.乙烯为平面结构,所有原子共平面,乙烯分子的球棍模型为: ,故D正确;
,故D正确;
故选A.
 ,故A错误;
,故A错误;B.氯离子核电荷数为17,最外层达到8电子稳定结构,Cl-的离子结构示意图为:
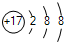 ,故B正确;
,故B正确;C.甲烷分子中存在4个碳氢键,为正四面体结构,碳原子半径大于氢原子,甲烷的球棍模型为:
 ,故C正确;
,故C正确;D.乙烯为平面结构,所有原子共平面,乙烯分子的球棍模型为:
 ,故D正确;
,故D正确;故选A.
点评:本题考查了常见化学用语的表示方法,题目难度中等,注意掌握结构简式、比例模型、离子结构示意图、电子式等化学用语的表示方法,试题培养了学生规范答题的能力.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
下列关于金属腐蚀的说法中不正确的是( )
| A、金属腐蚀的本质是金属原子失去电子而被氧化 |
| B、金属腐蚀一般包括化学腐蚀和电化学腐蚀 |
| C、纯的金属一般难以发生电化学腐蚀 |
| D、镀锌铁当镀层破损后,镀层则对铁失去了保护作用 |
氢键既可以存在于分子之间,也可以存在于分子内部的原子团之间,如邻羟基苯甲醛分子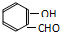 ) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子(
) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子( 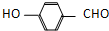 )之间存在氢键(分子间氢键).则两者的熔点、沸点的相对大小关系是( )
)之间存在氢键(分子间氢键).则两者的熔点、沸点的相对大小关系是( )
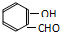 ) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子(
) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子(  )之间存在氢键(分子间氢键).则两者的熔点、沸点的相对大小关系是( )
)之间存在氢键(分子间氢键).则两者的熔点、沸点的相对大小关系是( )| A、前者>后者 | B、前者<后者 |
| C、前者=后者 | D、无法估计 |
下列有关阿伏加德罗常数(NA)的说法不正确的是( )
| A、0.012 kg12C所含有的碳原子数为NA个 |
| B、NA的近似值为6.02×1023 |
| C、1 mol H2O含有的H2O分子数目为NA个 |
| D、NA个Cl2的质量为35.5 g |
能正确表示下列反应的离子方程式是( )
| A、Ba(OH)2与稀H2SO4反应 Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| B、饱和碳酸钠溶液中通入足量CO2 CO32-+H2O+CO2═2HCO3- |
| C、C12与NaOH溶液反应 Cl2+2OH-═C1-+C1O-+H2O |
| D、把金属铁放入稀硫酸中 2Fe+6H+═2Fe3++3H2↑ |
在同温同压下,某集气瓶充满CO2时,质量为211g,充满N2时,质量为207g,若将该集气瓶改充H2,质量为( )
| A、200g |
| B、200.5g |
| C、201g |
| D、201.5g |