题目内容
在同温同压下,某集气瓶充满CO2时,质量为211g,充满N2时,质量为207g,若将该集气瓶改充H2,质量为( )
| A、200g |
| B、200.5g |
| C、201g |
| D、201.5g |
考点:物质的量的相关计算
专题:计算题
分析:同温同压下,相同容积时,气体的物质的量相同.令气体的物质的量为n,容器质量为m,根据容器充满二氧化碳与氧气的质量,列方程计算n、m的值,再根据m=nM计算氢气质量,进而计算充满氢气时的质量.
解答:
解:令气体的物质的量为n,容器质量为m,则:
m+n×44g/mol=211g
m+n×28g/mol=207g
解得,n=0.25mol,m=200g.
充满气体氢气后的质量为200g+0.25mol×2g/mol=200.5g,
故选B.
m+n×44g/mol=211g
m+n×28g/mol=207g
解得,n=0.25mol,m=200g.
充满气体氢气后的质量为200g+0.25mol×2g/mol=200.5g,
故选B.
点评:考查阿伏伽德罗定律及推论的计算,难度不大,确定气体的物质的量相等是解题关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质:①浓硫酸 ②HNO3 ③Cl2 ④H2 ⑤O2 ⑥Ag ⑦浓盐酸⑧KMnO4 ⑨MnO2 ⑩CO,其中属于常见氧化剂的一组是( )
| A、①②③④⑤⑧⑨ |
| B、①②③⑤⑧⑨ |
| C、①②③⑤⑥⑦⑧ |
| D、①②③⑤⑦⑨⑩ |
下列表示方法错误的是( )
A、氮分子的电子式: |
B、Cl-的离子结构示意图: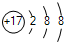 |
C、甲烷分子的比例模型: |
D、乙烯分子的球棍模型: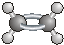 |
下列解释实际应用的原理表达式中,不正确的是( )
| A、用排饱和食盐水法收集Cl2:Cl2+H2O?H++Cl-+HClO |
| B、热的纯碱溶液碱性增强:CO32-+2H2O?H2CO3+2OH- |
| C、向Mg(OH)2悬浊液中加入FeCl3溶液:3Mg(OH)2(s)+2Fe3+═2 Fe(OH)3(s)+3Mg2+ |
| D、配制FeCl3溶液时为防止溶液浑浊加入少量稀盐酸Fe3++3H2O?Fe(OH)3+3H+ |
下列变化不能说明发生了化学变化的是( )
| A、变化时有电子的得失或共用电子对的偏移 |
| B、变化过程中有旧化学键的断裂和新化学键的形成 |
| C、变化时释放出能量 |
| D、变化前后原子的种类和数目没有改变,分子种类增加了 |
下列说法正确的是( )
| A、醋酸在醋酸钠溶液中电离程度大于在纯水中电离程度 | ||
| B、常温下0.1mol?L-1醋酸溶液的pH=a,加入适量的醋酸钠固体,能使溶液的pH=(a+1) | ||
| C、常温下由0.1mol?L-1一元碱BOH溶液的pH=10,推知该溶液中存在BOH=B++OH- | ||
D、向0.1mol?L-1的氨水中加入少量硫酸铵固体,则溶液中
|
两种气态烃组成的混合气体0.1mol,完全燃烧得0.16mol CO2和3.6g水,下列说法正确的是( )
| A、混和气体中一定有CH4 |
| B、混和气体中一定有甲烷和乙烯 |
| C、混和气体中一定没有乙烷 |
| D、混和气体中一定有乙炔 |

 具有的性质叙述正确的是
具有的性质叙述正确的是