题目内容
下列关于金属腐蚀的说法中不正确的是( )
| A、金属腐蚀的本质是金属原子失去电子而被氧化 |
| B、金属腐蚀一般包括化学腐蚀和电化学腐蚀 |
| C、纯的金属一般难以发生电化学腐蚀 |
| D、镀锌铁当镀层破损后,镀层则对铁失去了保护作用 |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:A、金属腐蚀的原理:金属失去电子发生氧化反应;
B、金属腐蚀的类型:一般包括化学腐蚀和电化学腐蚀;
C、纯的金属很难发生电化学腐蚀;
D、金属锌和铁构成的原电池中,金属锌是负极,易被腐蚀.
B、金属腐蚀的类型:一般包括化学腐蚀和电化学腐蚀;
C、纯的金属很难发生电化学腐蚀;
D、金属锌和铁构成的原电池中,金属锌是负极,易被腐蚀.
解答:
解:A、金属腐蚀的原理:金属失去电子发生氧化反应,是金属被还原的过程,故A正确;
B、金属腐蚀的类型:一般包括化学腐蚀和电化学腐蚀两种,故B正确;
C、纯的金属很难发生电化学腐蚀,因为不会构成原电池装置,故C正确;
D、镀锌铁当镀层破损后,金属锌和铁构成的原电池中,金属锌是负极,易被腐蚀,金属铁被保护,故D错误.
故选D.
B、金属腐蚀的类型:一般包括化学腐蚀和电化学腐蚀两种,故B正确;
C、纯的金属很难发生电化学腐蚀,因为不会构成原电池装置,故C正确;
D、镀锌铁当镀层破损后,金属锌和铁构成的原电池中,金属锌是负极,易被腐蚀,金属铁被保护,故D错误.
故选D.
点评:本题考查学生原电池的工作原理以及金属的腐蚀和防护知识,难度不大.

练习册系列答案
相关题目
钠及其化合物的下列用途与化学性质有关的是( )
| A、制焰火 |
| B、作原子反应堆的导热剂 |
| C、冶炼金属钛 |
| D、应用在电光源 |
100mL 6mol?L-1H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
| A、碳酸钠(s) |
| B、硫酸钠(s) |
| C、醋酸钠(s) |
| D、硫酸铵(s) |
在25℃时.密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如表:
下列说法错误的是( )
| 物质 | X | Y | Z |
| 初始浓度/mol?-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol?-1 | 0.05 | 0.05 | 0.1 |
| A、反应达到平衡时,X的转化率为50% |
| B、改变温度可以改变此反应的平衡常数 |
| C、增大压强使平衡向生成Z的方向移动,平衡常数增大 |
| D、反应可表示为X+3Y?2Z,其平衡常数为1600 |
锌铜原电池产生电流时,阴离子( )
| A、移向Zn极,阳离子移向Cu极 |
| B、移向Cu极,阳离子移向Zn极 |
| C、和阳离子都移向Zn极 |
| D、和阳离子都移向Cu极 |
下列物质:①浓硫酸 ②HNO3 ③Cl2 ④H2 ⑤O2 ⑥Ag ⑦浓盐酸⑧KMnO4 ⑨MnO2 ⑩CO,其中属于常见氧化剂的一组是( )
| A、①②③④⑤⑧⑨ |
| B、①②③⑤⑧⑨ |
| C、①②③⑤⑥⑦⑧ |
| D、①②③⑤⑦⑨⑩ |
下列表示方法错误的是( )
A、氮分子的电子式: |
B、Cl-的离子结构示意图: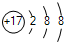 |
C、甲烷分子的比例模型: |
D、乙烯分子的球棍模型: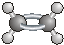 |
 在一固定容积的密闭容器中进行着反应:CO2(g)+H2(g)?CO(g)+H2O(g),其平衡常数K和温度的关系如下:
在一固定容积的密闭容器中进行着反应:CO2(g)+H2(g)?CO(g)+H2O(g),其平衡常数K和温度的关系如下: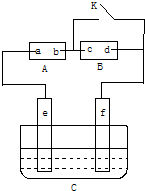 如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,填空:
如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,填空: