题目内容
1.以乙炔为原料通过以下流程能合成有机物中间体D.C2H2$→_{①}^{HCHO}$A(HOH2OC≡OCH2OH)$→_{②}^{足量H_{2}}$B$→_{③}^{O_{2}}$C$→_{④}^{稀NaOH}$D(
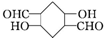 )
)已知:(1)
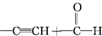 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$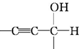
(2)
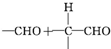 $\stackrel{稀NaOH}{→}$
$\stackrel{稀NaOH}{→}$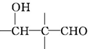
请回答下列问题:
(1)化合物D的分子式为C8H12O4,写出D中一种官能团的名称:羟基或醛基.
(2)写出生成A的反应的化学方程式:HC≡CH+2HCHO$\stackrel{一定条件下}{→}$HOCH2C≡CCH2OH.
(3)化合物B在浓硫酸催化下,加热与HOOCCOOH反应生成环状酯的化学方程式为
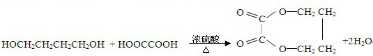 (注明条件).
(注明条件).(4)化合物C的结构简式为OHCCH2CH2CHO.
(5)已知1mol HCHO和1mol CH3CH2CHO发生类似已知(2)的反应,生成1mol E.以下关于E的说法正确的是ac.
a.E能与H2发生加成反应,也能使酸性高锰酸钾溶液褪色
b.E属于酯类物质
c.1mol E完全燃烧消耗5mol O2
d.生成E的反应属于取代反应.
分析 乙炔和甲醛发生加成反应生成A,A与足量氢气反应生成B为HOCH2CH2CH2CH2OH,B发生氧化反应生成C,
C为OHCCH2CH2CHO,C发生信息(2)的反应生成D,
1mol HCHO和1mol CH3CH2CHO发生类似已知(2)的反应,生成1molE,E为HOCH2CH(CH3)CHO,结合对应的物质的性质以及题目要求解答该题.
解答 解:乙炔和甲醛发生加成反应生成A,A与足量氢气反应生成B为HOCH2CH2CH2CH2OH,B发生氧化反应生成C,
C为OHCCH2CH2CHO,C发生信息(2)的反应生成D,
1mol HCHO和1mol CH3CH2CHO发生类似已知(2)的反应,生成1molE,E为HOCH2CH(CH3)CHO,
(1)根据结构简式知,D分子式为C8H12O4,D中官能团为羟基和醛基,故答案为:C8H12O4;羟基或醛基;
(2)甲醛和乙炔在一定条件下反应生成A,反应方程式为HC≡CH+2HCHO$\stackrel{一定条件下}{→}$HOCH2C≡CCH2OH,故答案为:HC≡CH+2HCHO$\stackrel{一定条件下}{→}$HOCH2C≡CCH2OH;
(3)B为HOCH2CH2CH2CH2OH,加热与HOOCCOOH反应生成环状酯的化学方程式为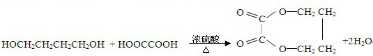 ,
,
故答案为: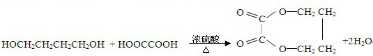 ;
;
(4)通过以上分析知,C为OHCCH2CH2CHO,故答案为:OHCCH2CH2CHO;
(5)E为HOCH2CH(CH3)CHO,
a.E中含有醛基和醇羟基,醛基能和氢气发生加成反应,所以E能与H2发生加成反应,醛基能被酸性高锰酸钾溶液氧化,所以也能使酸性高锰酸钾溶液褪色,故正确;
b.E中不含酯基,所以不属于酯类物质,故错误;
c.1molE完全燃烧消耗O2为(4+$\frac{8}{4}$-1)mol=5mol,故正确;
d.生成E的反应属于加成反应,故错误;
故选ac.
点评 本题考查有机物的推断和合成,为高考常见题型,侧重于考查学生分析能力、推断能力和综合运用化学知识的能力,题目难度中等,注意把握题给信息.

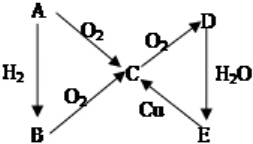 (有些反应条件均已省略,如加热、点燃等)则A的化学式可能是( )
(有些反应条件均已省略,如加热、点燃等)则A的化学式可能是( )| A. | N2 | B. | Cl2 | C. | S | D. | C |
①失电子能力:K>Na>Li ②碱性:NaOH>Mg(OH)2>Al(OH)3 ③氧化性:F>Si>O ④稳定性:PH3<H2S<HCl.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
| A. |  根据图可判断可逆反应A2(g)+3B2(g)═2AB3(g)的△H>0 | |
| B. | 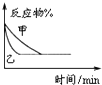 表示压强对可逆反应2A(g)+2B(g)═3C(g)+D(s)的影响,乙的压强大 | |
| C. | 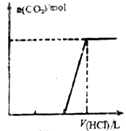 表示在含等物质的量NaOH、Na2CO3的混合溶液中逐滴加入0.1mol/L盐酸至过量时,产生气体的物质的量与消耗盐酸的体积关系 | |
| D. | 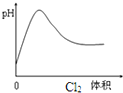 表示Cl2通入H2S溶液中pH变化 |
| A. | ①②③④ | B. | ①②③ | C. | ①② | D. | ①③ |
| 选项 | Na2B2O7 | CaF2 | H3BO3 | NH3 |
| A | 原子晶体 | 金属晶体 | 原子晶体 | 分子晶体 |
| B | 离子晶体 | 分子晶体 | 离子晶体 | 分子晶体 |
| C | 离子晶体 | 离子晶体 | 分子晶体 | 分子晶体 |
| D | 分子晶体 | 离子晶体 | 分子晶体 | 离子晶体 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 单质硅是将太阳能转化为电能的常用材料 | |
| B. | 大气中SO2是形成酸雨的主要因素之一 | |
| C. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 | |
| D. | “血液透析”利用了胶体的性质 |
| A. | 常温下干燥的Cl2能用钢瓶贮运 | |
| B. | 检验HCl气体中是否混有Cl2,方法是将气体通入硝酸银溶液 | |
| C. | 自然界中不存在游离态硅 | |
| D. | HF溶液不能贮存在磨口玻璃塞的试剂瓶中 |