籾朕坪否
12⤴和双光怏來嵎曳熟嶄⇧屎鳩議頁↙ ⇄〙払窮徨嬬薦⦿K﹅Na﹅Li 〖珠來⦿NaOH﹅Mg↙OH⇄2﹅Al↙OH⇄3 〗剳晒來⦿F﹅Si﹅O ∠糧協來⦿PH3〽H2S〽HCl⤴
| A⤴ | 〙〖〗 | B⤴ | 〖〗∠ | C⤴ | 〙〖∠ | D⤴ | 〙〗∠ |
蛍裂 圷殆議署奉來埆膿⇧凪圻徨払窮徨嬬薦埆膿、凪斤哘剳晒麗議邦晒麗珠來埆膿◉圷殆議掲署奉來埆膿⇧凪誼窮徨嬬薦埆膿⇧夸圷殆議剳晒來埆膿、凪狽晒麗議糧協來埆膿⇧象緩蛍裂盾基⤴
盾基 盾⦿圷殆議署奉來埆膿⇧凪圻徨払窮徨嬬薦埆膿、凪斤哘剳晒麗議邦晒麗珠來埆膿◉圷殆議掲署奉來埆膿⇧凪誼窮徨嬬薦埆膿⇧夸圷殆議剳晒來埆膿、凪狽晒麗議糧協來埆膿⇧
〙署奉來⦿K﹅Na﹅Li⇧夸払窮徨嬬薦⦿K﹅Na﹅Li⇧絞屎鳩◉
〖署奉來⦿Na﹅Mg﹅Al⇧夸珠來⦿NaOH﹅Mg↙OH⇄2﹅Al↙OH⇄3 ⇧絞屎鳩◉
〗掲署奉來⦿F﹅O﹅Si⇧夸剳晒來⦿F﹅O﹅Si⇧絞危列◉
∠掲署奉來⦿Cl﹅S﹅P⇧夸糧協來⦿PH3〽H2S〽HCl⇧絞屎鳩
絞僉C⤴
泣得 云籾深臥阻圷殆巓豚舵議哘喘⇧苧鳩圷殆巓豚舵坪梱頁盾云籾購囚⇧功象揖匯巓豚、揖匯麼怛圷殆議弓延來栖蛍裂盾基⇧籾朕佃業音寄⤴

膳楼過狼双基宛
屢購籾朕
20⤴﨑100mL喇吉麗嵎議楚議FeBr2才FeI2塘撹議詞栽卑匣嶄⇧産蛸宥秘柁賑3.36L↙炎彈彜趨⇄⇧郡哘頼畠朔⇧卑匣嶄嗤匯磯議Fe2+瓜剳晒撹Fe3+⇧夸圻詞栽匣嶄FeI2議麗嵎議楚敵業葎↙ ⇄
| A⤴ | 0.5 moL•L-1 | B⤴ | 1.0 moL•L-1 | C⤴ | 1.2 moL•L-1 | D⤴ | 1.5 moL•L-1 |
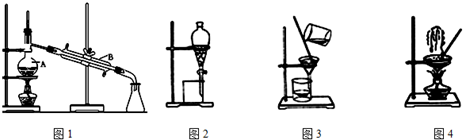
3⤴和双蛍宣圭隈屎鳩議頁↙ ⇄
| A⤴ | 喘卑盾朔狛陀議圭隈茅肇CaCl2嶄議富楚議ZnSO4 | |
| B⤴ | 喘殕函議圭隈蛍宣NaCl卑匣才廿嗟 | |
| C⤴ | 喘焼娼殕函汲邦嶄議汲 | |
| D⤴ | 喘對蒼議圭隈茅肇邦嶄議音屍窟議墫嵎 |
20⤴和双夕幣議晒僥糞刮荷恬嶄⇧屎鳩議頁↙ ⇄
| A⤴ | 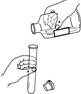 買宜匣悶 | B⤴ | 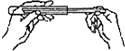 函頚挑彜耕悶勞瞳 | ||
| C⤴ | 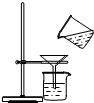 狛陀 | D⤴ | 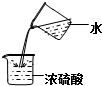 敵葬磨議蓮瞥 |
7⤴NA旗燕唖懸紗蟻袋械方議峙⤴和双偃峰屎鳩議頁↙屢斤圻徨嵎楚⦿Fe---56⇄↙ ⇄
| A⤴ | 菰鑓窟伏裂狽遣粉扮⇧0.56gFe郡哘 廬卞窮徨方葎0.03NA | |
| B⤴ | 1L 0.1mol•L-1議NaHCO3卑匣嶄HCO3-才CO32-宣徨方岻才葎0.1NA | |
| C⤴ | 1molH2O2蛍徨嶄議掲自來慌勺囚 1NA | |
| D⤴ | 狽剳伴創窮学屎自嶧債22.4L賑悶扮⇧窮揃嶄宥狛議窮徨方朕葎4 NA |
2⤴X、Y、Z譲葎玉巓豚圷殆⇧X、Y侃噐揖匯巓豚⇧X、Z議恷詰勺宣徨蛍艶葎X2-才Z-⇧Y+才Z-醤嗤屢揖議窮徨蚊潤更⇧和双傍隈屎鳩議頁↙ ⇄
| A⤴ | 圻徨恷翌蚊窮徨方⦿Z﹅Y﹅X | B⤴ | 汽嵎畜業⦿Y﹅X﹅Z | ||
| C⤴ | 宣徨磯抄⦿X2-﹅Z-﹅Y+ | D⤴ | 圻徨會方⦿X﹅Z﹅Y |
 ⇄
⇄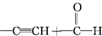 $\stackrel{匯協訳周}{★}$
$\stackrel{匯協訳周}{★}$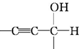
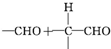 $\stackrel{蓮NaOH}{★}$
$\stackrel{蓮NaOH}{★}$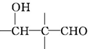
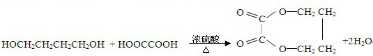 ↙廣苧訳周⇄⤴
↙廣苧訳周⇄⤴