题目内容
1.用NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 71g氯气与过量的FeCl2溶液完全反应转移的电子数为2NA | |
| B. | 1 mol甲基(-14CH3)所含中子数为9NA | |
| C. | 在标准状况下,2.24L四氯甲烷所含的分子数为0.1NA | |
| D. | 2L 0.1mol/L 的醋酸钠溶液中,所含离子总数是0.2NA |
分析 A、求出氯气的物质的量,然后根据反应后氯元素变为-1价来分析;
B、根据甲基中为14C来分析;
C、标况下,四氯化碳为液态;
D、根据溶液中电荷守恒来分析.
解答 解:A、71g氯气的物质的量为1mol,而反应后氯元素变为-1价,故1mol氯气转移2mol电子,即2NA个,故A正确;
B、甲基中为14C,故碳原子中的中子数为14-6=8,而氢原子中不含中子,故1mol(-14CH3)中含8mol中子,即8NA个电子,故B错误;
C、标况下,四氯化碳为液态,故不能根据气体摩尔体积来计算,故C错误;
D、溶液中各离子要满足电荷守恒:n(Na+)+n(H+)=n(OH-)+n(CH3COO-),而n(Na+)=CV=0.1mol/L×2L=0.2mol,故n(Na+)+n(H+)=n(OH-)+n(CH3COO-)>0.2mol,则溶液中的离子的总物质的量大于0.4mol,即大于0.4NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
7.熔融碳酸盐燃料电池(MCFC)是使用熔融碳酸锂、碳酸钾作电解质的一种新型电池,该电池的工作温度为650℃.负极由镍铬铝合金烧结而成,正极材料为多孔镍,电池反应为:H2+CO+O2=CO2+H2O.下列说法正确的是( )
| A. | 负极反应Al-3e-Al3+ | B. | 燃料气体是氧气 | ||
| C. | 正极反应为2CO2+O2+4e-2CO32- | D. | 该电池不能用烃类物质作燃料 |
12.用含有Al2O3、SiO2和少量FeO•xFe2O3的铝灰制备Al2(SO4)3•18H2O.制备步骤如下(部分操作和条件略):
I.向铝灰中加入过量稀H2SO4,过滤;
II.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
III.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
IV.加入MnSO4至紫红色消失,过滤;
V.浓缩、结晶、分离,得到产品.
(1)步骤Ⅰ过滤得到沉淀的主要成分SiO2(填化学式),H2SO4溶解Al2O3的离子方程式是Al2O3+6H+=2Al3++3H2O.
(2)已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol•L-1
根据表中数据解释步骤II的目的pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀.
(3)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+2H2O+Cl2↑
②Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
I.向铝灰中加入过量稀H2SO4,过滤;
II.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
III.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
IV.加入MnSO4至紫红色消失,过滤;
V.浓缩、结晶、分离,得到产品.
(1)步骤Ⅰ过滤得到沉淀的主要成分SiO2(填化学式),H2SO4溶解Al2O3的离子方程式是Al2O3+6H+=2Al3++3H2O.
(2)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤II的目的pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀.
(3)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+2H2O+Cl2↑
②Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
9.下列反应不属于消去反应的是( )
| A. | CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O | |
| B. | CH3CHBrCH3+NaOH$→_{△}^{乙醇}$CH3CH═CH2↑+NaBr+H2O | |
| C. | 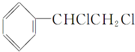 +2NaOH$→_{△}^{乙醇}$ +2NaOH$→_{△}^{乙醇}$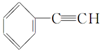 +2NaCl+2H2O +2NaCl+2H2O | |
| D. | 2CH3OH$→_{△}^{浓硫酸}$CH3-O-CH3+H2O |
16. 据媒体报道,一些非法油厂用大豆油、棕榈油、粗制棉油等添加香精勾兑成花生油.如图就是一种香精的结构,下列对该香精的叙述不正确的是( )
据媒体报道,一些非法油厂用大豆油、棕榈油、粗制棉油等添加香精勾兑成花生油.如图就是一种香精的结构,下列对该香精的叙述不正确的是( )
 据媒体报道,一些非法油厂用大豆油、棕榈油、粗制棉油等添加香精勾兑成花生油.如图就是一种香精的结构,下列对该香精的叙述不正确的是( )
据媒体报道,一些非法油厂用大豆油、棕榈油、粗制棉油等添加香精勾兑成花生油.如图就是一种香精的结构,下列对该香精的叙述不正确的是( )| A. | 该香精能够水解,其水解产物中有醇 | |
| B. | 该香精能够使酸性KMnO4溶液褪色 | |
| C. | 该香精能够与溴水发生加成反应 | |
| D. | 1 mol该香精中含有1 mol碳氧双键和4 mol碳碳双键 |
6.某些电解质分子的中心原子最外层电子未达饱和结构,其电离采取结合溶液中其他离子的形式,而使中心原子最外层电子达到饱和结构.例如:硼酸分子的中心原子B最外层电子并未达到饱和,它在水中的电离过程为:
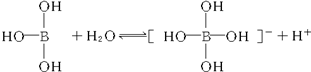
下列判断正确的是( )
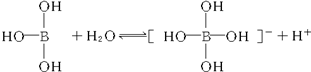
下列判断正确的是( )
| A. | 凡是酸或碱对水的电离都是抑制的 | |
| B. | 硼酸分子中除氢原子外每个其他原子最外层都满足8电子稳定结构 | |
| C. | 硼酸溶液与NaOH溶液反应的离子方程式为:H3BO3+OH-═[B(OH)4]- | |
| D. | 硼酸是两性化合物 |
13.对于10mL 1mol/L盐酸与锌粒的反应,采取下列措施能使反应速率加快的是( )
①升高温度; ②改用10mL 3mol/L盐酸; ③改用30mL 1mol/L醋酸;
④用等量锌粉代替锌粒; ⑤改用10mL 3mol/L硝酸.
①升高温度; ②改用10mL 3mol/L盐酸; ③改用30mL 1mol/L醋酸;
④用等量锌粉代替锌粒; ⑤改用10mL 3mol/L硝酸.
| A. | ①②④ | B. | ①③④⑤ | C. | ①②③④ | D. | ①②④⑤ |
10.在${\;}_{m}^{n}$X${\;}_{q}^{p}$ 中,m、n、p、q表示某种元素X的四个角码,若X1与X2的q均为1,m、p的值相等,而n值不相等,则X1和X2表示的可能是( )
| A. | 不同的原子 | B. | 同一元素的不同原子或离子 | ||
| C. | 不同元素的离子 | D. | 不同的元素 |