题目内容
1.以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为硫的价类图,例如d点可表示+6价的硫酸盐.下列说法错误的是( )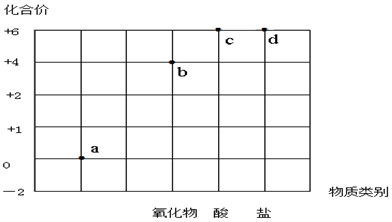
| A. | a点表示的物质所属的物质类别是单质 | |
| B. | b点表示的物质可以是SO2或SO3 | |
| C. | c点表示的化合物的浓溶液可作为干燥剂 | |
| D. | d点表示的可溶性物质能与BaCl2溶液发生反应 |
分析 A、根据单质中元素的化合价为零考虑;
B、由表知b点是+4价的氧化物;
C、c点表示的化合物的浓溶液是浓硫酸;
D、可溶性的硫酸盐与氯化钡发生复分解反应.
解答 解:A、根据单质中元素的化合价为零考虑,所以a点表示的物质所属的物质类别是单质,故A正确;
B、b点是+4价的氧化物所以b点表示的物质是SO2,故B错误;
C、浓硫酸是干燥剂,故C正确;
D、可溶性的硫酸盐与氯化钡发生复分解反应,生成硫酸钡沉淀,故D正确;
故选B.
点评 本题考查硫的化合物的性质,解答本题关键是要知道单质中元素的化合价是零,在化合物中正负化合价代数和为零,熟悉硫的化合物的性质.

练习册系列答案
相关题目
12.下列叙述不正确的是( )
| A. | 胶体区别于其它分散系的本质特征是:胶体粒子直径在1-100nm之间 | |
| B. | 一定温度、压强下,气体体积由其分子的大小决定 | |
| C. | 氧化还原反应的本质是电子转移 | |
| D. | 在1L2mol/L的氢氧化铁胶体中含有氢氧化铁胶粒数小于2NA |
9.如图所示铜锌原电池T作时,下列叙述不正确的是( )
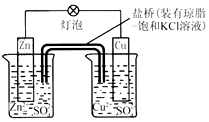

| A. | 负极反应为:2n-2e -═2n2+ | B. | 电池反应为:Zn+Cu2+═Zn2++Cu | ||
| C. | 盐桥中酌K+移向ZnSO4溶液 | D. | 在外电路中,电子从负极流向正极 |
16.下列有关阿佛加德罗常数(NA)的说法错误的是( )
| A. | 0.5molH2O含有的原子数目为1.5NA | B. | 0.5molNH3含有的电子数目为4NA | ||
| C. | 28gCO含有的分子数目为NA | D. | 2NA个氯气分子的物质的量是2mol |
6.下列说法中不正确的是( )
| A. | 向沸腾的蒸馏水中逐滴加入FeCl3饱和溶液,至液体呈透明的红褐色即可制得氢氧化铁胶体 | |
| B. | 观察是一种有计划、有目的地用感官考察研究对象的方法 | |
| C. | 在豆浆中加入盐卤做豆腐利用的是胶体聚沉的原理 | |
| D. | 研究物质性质的一般程序的第一步是预测物质的性质 |
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L 四氯化碳(CCl4)含有的碳原子数目为NA | |
| B. | CO2通过Na2O2使其增重5.6g时,反应中转移的电子数为0.4 NA | |
| C. | 0.2mol Fe与0.2 mol Cl2反应时失电子数为0.6NA | |
| D. | 常温常压下,29.8 g KCl与NaClO的固体混合物中阴离子的数目为0.4 NA |
10.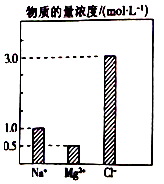 在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分,下列说法不正确的是( )
在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分,下列说法不正确的是( )
 在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分,下列说法不正确的是( )
在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分,下列说法不正确的是( )| A. | NaCl的物质的量为0.2mol | |
| B. | 溶质MgCl2的质量为9 g | |
| C. | 该混合液中BaCl2的物质的量为0.1mol | |
| D. | 将该混合液加水稀释至体积为1 L,稀释后溶液中的Ba2+物质的量浓度为0.1mol/L |