题目内容
9.如图所示铜锌原电池T作时,下列叙述不正确的是( )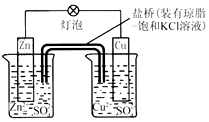
| A. | 负极反应为:2n-2e -═2n2+ | B. | 电池反应为:Zn+Cu2+═Zn2++Cu | ||
| C. | 盐桥中酌K+移向ZnSO4溶液 | D. | 在外电路中,电子从负极流向正极 |
分析 锌、铜和硫酸铜、硫酸锌组成的原电池中,锌作负极,负极上锌失电子发生氧化反应;铜作正极,正极上铜离子得电子发生还原反应;电子从负极沿导线流向正极;阳离子移向正极,阴离子移向负极.
解答 解:A、锌、铜和硫酸铜、硫酸锌组成的原电池中,锌作负极,负极上锌失电子发生氧化反应,反应为:Zn-2e -═Zn2+,故A正确;
B、锌、铜和硫酸铜、硫酸锌组成的原电池中,锌作负极,铜作正极,电池反应为:Zn+Cu2+═Zn2++Cu,故B正确;
C、盐桥中的K+移向正极CuSO4溶液,故C错误;
D、锌、铜和硫酸铜、硫酸锌组成的原电池中,电子从负极沿导线流向正极,故D正确;
故选C.
点评 本题考查学生原电池的工作原理,注意把握正负极的判断、电极方程式的书写、电子流向等,题目难度不大.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
19.用已知浓度的NaOH溶液测定未知浓度的盐酸(滴定时盐酸置于酸式滴定管中),以下操作会造成所测盐酸溶液浓度偏高的是( )
| A. | 酸式滴定管未用待测溶液润洗 | |
| B. | 碱式滴定管未用待装溶液润洗 | |
| C. | 锥形瓶未用待装溶液润洗 | |
| D. | 在滴定前滴定管尖嘴部分有气泡,滴定后气泡消失 |
20.下列指定反应的离子方程式正确的是( )
| A. | Cl2通入水中:Cl2+H2O=2H++Cl-+ClO- | |
| B. | 铜丝插入稀硝酸:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | |
| C. | 向NaClO溶液中通入过量SO2:ClO-+SO2+H2O=HClO+HSO3- | |
| D. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
17.世博园地区改造前,规划区内有一座大型钢铁厂,附近居民曾饱受到该厂产生的棕红色烟雾的困扰.估计这一空气污染物可能含有( )
| A. | FeO粉尘 | B. | Fe3O4粉尘 | C. | Fe2O3粉尘 | D. | NO2气体 |
4.下列原子半径由小到大排列顺序正确的是( )
| A. | O、S、Na | B. | Mg、P、Cl | C. | Cl、Na、F | D. | S、N、C |
14.已知金属钠化学性质活泼,能跟多种物质发生反应,其中包括与酒精在常温下反应.要研究金属钠分别与酒精和水反应的异同点,下列研究方法中用不到的是( )
| A. | 实验法 | B. | 分类法 | C. | 观察法 | D. | 比较法 |
1.以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为硫的价类图,例如d点可表示+6价的硫酸盐.下列说法错误的是( )
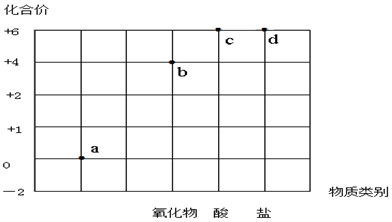

| A. | a点表示的物质所属的物质类别是单质 | |
| B. | b点表示的物质可以是SO2或SO3 | |
| C. | c点表示的化合物的浓溶液可作为干燥剂 | |
| D. | d点表示的可溶性物质能与BaCl2溶液发生反应 |
18.以NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2L的水中水分子数为0.5NA | |
| B. | 通常状况下,0.5NA个氮分子占有的体积为11.2L | |
| C. | 1molH2和O2的混合气体中含2NA个分子 | |
| D. | 0.1mol的OH-中含有的电子数为NA |