题目内容
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,22.4 L 四氯化碳(CCl4)含有的碳原子数目为NA | |
| B. | CO2通过Na2O2使其增重5.6g时,反应中转移的电子数为0.4 NA | |
| C. | 0.2mol Fe与0.2 mol Cl2反应时失电子数为0.6NA | |
| D. | 常温常压下,29.8 g KCl与NaClO的固体混合物中阴离子的数目为0.4 NA |
分析 A、标况下四氯化碳为液态;
B、二氧化碳和过氧化钠反应时,当增重28g时,转移1mol电子;
C、0.2mol铁和0.2mol氯气反应时,铁过量,氯气完全反应后变为-1价;
D、KCl与NaClO的摩尔质量均为74.5g/mol,且均由一个阳离子和一个阴离子构成.
解答 解:A、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、二氧化碳和过氧化钠反应时,当增重28g时,转移1mol电子,故当增重5.6g时,转移0.2mol电子即0.2NA个,故B错误;
C、0.2mol铁和0.2mol氯气反应时,铁过量,氯气完全反应后变为-1价,故0.2mol氯气得0.4NA个电子,则铁失去0.4NA个电子,故C错误;
D、KCl与NaClO的摩尔质量均为74.5g/mol,故29.8g混合物的物质的量为0.4mol,且两者均由一个阳离子和一个阴离子构成,故0.4mol混合物中含阴离子为0.4NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列说法正确的是( )
| A. | 已知X、Y元素同周期,且电负性X>Y,则第一电离能X大于Y | |
| B. | 分子中键能越大,键长越短,则分子越稳定,熔沸点越高 | |
| C. | N-H键键能的含义是拆开约6.02×1023个N-H键所吸收的能量 | |
| D. | H2O中每个O原子结合2个H原子的根本原因是共价键具有方向性 |
4.下列原子半径由小到大排列顺序正确的是( )
| A. | O、S、Na | B. | Mg、P、Cl | C. | Cl、Na、F | D. | S、N、C |
1.以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为硫的价类图,例如d点可表示+6价的硫酸盐.下列说法错误的是( )
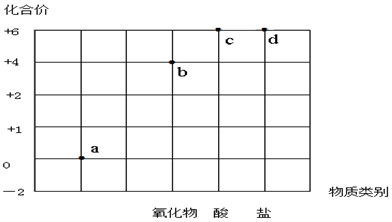

| A. | a点表示的物质所属的物质类别是单质 | |
| B. | b点表示的物质可以是SO2或SO3 | |
| C. | c点表示的化合物的浓溶液可作为干燥剂 | |
| D. | d点表示的可溶性物质能与BaCl2溶液发生反应 |
8.2a L Fe2(SO4)3和(NH4)2SO4的混合液分成两等份,向其中一份加入bmol的BaCl2溶液,恰好使溶液中的SO42-完全沉淀:向另一等份加入足量NaOH固体可得到cmol Fe(OH)3沉淀,则原溶液中NH4+的物质的量浓度为______mol•L-1( )
| A. | $\frac{2b-3c}{2a}$ | B. | $\frac{2b-3c}{a}$ | C. | $\frac{2b-c}{3a}$ | D. | $\frac{2b-c}{6a}$ |
18.以NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2L的水中水分子数为0.5NA | |
| B. | 通常状况下,0.5NA个氮分子占有的体积为11.2L | |
| C. | 1molH2和O2的混合气体中含2NA个分子 | |
| D. | 0.1mol的OH-中含有的电子数为NA |