题目内容
12.下列属于吸热反应的是( )①冰雪融化 ②KMnO4分解制O2 ③铝与氧化铁的反应 ④钠与水反应 ⑤二氧化碳与灼热木炭反应 ⑥碘的升华 ⑦Ba(OH)2•8H2O和NH4Cl反应.
| A. | ②⑥⑦ | B. | ②⑤⑦ | C. | ①②⑤⑥⑦ | D. | ③④ |
分析 根据常见的放热反应有:所有的物质燃烧、金属与酸或水反应、中和反应、铝热反应、绝大多数化合反应等;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),八水合氢氧化钡与氯化铵的反应.
解答 解:①冰雪融化不是化学反应,故错误;
②KMnO4分解制O2 是分解反应,故为吸热反应,故正确;
③铝与氧化铁的反应是铝热反应,是放热反应,故错误;
④钠与水反应是放热反应,故错误;
⑤二氧化碳与灼热木炭反应是吸热反应,故正确;
⑥碘的升华不是反应,故错误;
⑦Ba(OH)2•8H2O和NH4Cl反应是吸热反应,故正确.
故选B.
点评 本题考查吸热反应和放热反应,难度不大,明确常见的吸热反应和放热反应是解题的关键.

练习册系列答案
相关题目
2.α-铁纳米粉在现代电子工业上用途广泛,用赤铁矿石(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO等)制备纳米铁颗粒的实验流程如下:
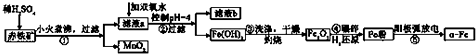
已知:部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
(1)步骤②滤液b中含有的金属阳离子是Cu2+、Al3+,步骤④中碾碎的目的是增大接触面积,提高原料的转化率和反应速率.
(2)将第①步过滤所得的MnO2与KClO3、KOH溶液共热,可得到K2MnO4和KCl,此反应的化学方程式是3MnO2+6KOH+KClO3=3K2MnO4+KCl+3H2O.
(3)步骤③灼烧所需的仪器有酒精灯、三脚架、泥三角、坩埚、坩埚钳.
(4)“纳米铁”在空气中受撞击时会燃烧,其反应与铁在纯氧中燃烧相同,写出该反应的化学方程式3Fe+2O2$\frac{\underline{\;撞击\;}}{\;}$Fe3O4.

已知:部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 |
(2)将第①步过滤所得的MnO2与KClO3、KOH溶液共热,可得到K2MnO4和KCl,此反应的化学方程式是3MnO2+6KOH+KClO3=3K2MnO4+KCl+3H2O.
(3)步骤③灼烧所需的仪器有酒精灯、三脚架、泥三角、坩埚、坩埚钳.
(4)“纳米铁”在空气中受撞击时会燃烧,其反应与铁在纯氧中燃烧相同,写出该反应的化学方程式3Fe+2O2$\frac{\underline{\;撞击\;}}{\;}$Fe3O4.
17.溶液、胶体和浊液这三种分散系的本质区别是( )
| A. | 是否为大量分子和离子的集合体 | B. | 能否通过滤纸或半透膜 | ||
| C. | 分散质粒子的大小 | D. | 是否均一、稳定、透明 |
4.下列物质分类全部正确的是( )
①纯碱 ②食盐水 ③石灰水 ④NaHSO4 ⑤液态氧 ⑥NaOH.
①纯碱 ②食盐水 ③石灰水 ④NaHSO4 ⑤液态氧 ⑥NaOH.
| A. | 盐--①④ | B. | 碱--①⑥ | C. | 纯净物--③④⑤ | D. | 混合物--②⑤ |
1.下列叙述正确的是(NA为阿伏加德罗常数的值)( )
| A. | 7.8gNa2O2含有的共价键数为0.2NA | |
| B. | 7.8gNa2S与Na2O2的混合物,含离子总数为0.3NA | |
| C. | 标准状况下,22.4L溴单质含有NA个溴分子 | |
| D. | 0.2 molNa被完全氧化生成7.8gNa2O2,转移电子的数目为0.4NA |