题目内容
2.α-铁纳米粉在现代电子工业上用途广泛,用赤铁矿石(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO等)制备纳米铁颗粒的实验流程如下: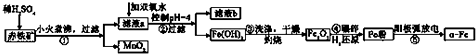
已知:部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 |
(2)将第①步过滤所得的MnO2与KClO3、KOH溶液共热,可得到K2MnO4和KCl,此反应的化学方程式是3MnO2+6KOH+KClO3=3K2MnO4+KCl+3H2O.
(3)步骤③灼烧所需的仪器有酒精灯、三脚架、泥三角、坩埚、坩埚钳.
(4)“纳米铁”在空气中受撞击时会燃烧,其反应与铁在纯氧中燃烧相同,写出该反应的化学方程式3Fe+2O2$\frac{\underline{\;撞击\;}}{\;}$Fe3O4.
分析 Fe2O3、FeO、Al2O3、CuO与硫酸反应,a中金属阳离子为Cu2+、Al3+、Fe2+、Fe3+,加双氧水将Fe2+氧化为Fe3+.根据阳离子沉淀时pH数据,可知控制pH=4时,铁离子已全部变成Fe(OH)3沉淀,滤液b中主要为Cu2+、Al3+,氢氧化铁洗涤干燥灼烧得到氧化铁,碾碎用氢气还原得到金属铁粉,利用电弧加热使金属熔融蒸发成蒸汽,使大量颗粒状烟灰尘与周围不反应的气体原子激烈碰撞进行充分的能量交换和电荷交换生成α-Fe,
(1)步骤②滤液中含有的金属阳离子是Cu2+、Al3+; 步骤④中碾碎的目的是增大接触面积,提高原料的转化率和反应速率;
(2)MnO2与KClO3、KOH溶液共热,MnO2做还原剂,生成K2MnO4,KClO3做氧化剂生成KCl;
(3)灼烧固体需酒精灯、三脚架、泥三角、坩埚、坩埚钳;
(4)“纳米铁”在空气中受撞击时会燃烧,其反应与铁在纯氧中燃烧相同,说明是生成了四氧化三铁.
解答 解:(1)步骤②滤液中含有的金属阳离子是Cu2+、Al3+; 步骤④中碾碎的目的是增大接触面积,提高原料的转化率和反应速率,
故答案为:Cu2+、Al3+; 增大接触面积,提高原料的转化率和反应速率;
(2)将第①步过滤所得的MnO2与KClO3、KOH溶液共热,可得到K2MnO4,MnO2做还原剂,生成K2MnO4,KClO3做氧化剂生成KCl,此反应的化学方程式是:
3MnO2+6KOH+KClO3=3 K2MnO4+KCl+3H2O,
故答案为:3MnO2+6KOH+KClO3=3 K2MnO4+KCl+3H2O;
(3)步骤③灼烧固体所需的仪器有酒精灯、三脚架、泥三角、坩埚、坩埚钳,
故答案为:坩埚、坩埚钳;
(4)“纳米铁”在空气中受撞击时会燃烧,其反应与铁在纯氧中燃烧相同,说明是生成了四氧化三铁,反应的化学方程式为:3Fe+2O2$\frac{\underline{\;撞击\;}}{\;}$Fe3O4,
故答案为:3Fe+2O2$\frac{\underline{\;撞击\;}}{\;}$Fe3O4.
点评 本题考查了物质分离、物质制备、实验基本操作、物质性质的理解应用等知识点,掌握基础是解题关键,题目难度中等

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案(1)松花蛋于明朝初年问世,其腌制配方有多种,但主要配料为生石灰(Ca0)、纯碱(Na2C03)和食盐(NaCl).将一定比例的配料用水和黏土调制成糊状,敷于蛋上,密封保存,数日后即可食用.
①将松花蛋外的糊状物用足量水溶解,溶解过程中反应的化学方程式分别为CaO+H2O=Ca(OH)2、Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
②某同学设计如表所示的实验方案,探究①中反应后过滤所得滤液中可能含有的物质,请你帮他完善实验方案.
| 实验步骤 | 实验现象 | 结论 |
| 取少量滤液,滴加适量K2CO3溶液 | 若出现白色沉淀 | 滤液中含Ca(OH)2 |
| 若无白色沉淀 | 滤液中无Ca(OH)2 | |
| 另取少量滤液,滴入适量盐酸 | 若出现气泡 | 滤液中含Na2CO3 |
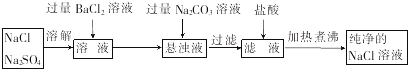
①氯化钡溶液不能(填“能”或“不能”)用硝酸钡溶液代替,理由是会引入新的杂质.
②加入碳酸钠溶液的目的是除去过量的Ba2+,为什么不先过滤而后加入碳酸钠溶液,理由是一次性过滤出硫酸钡和碳酸钡沉淀,避免重复操作.
| A. | 任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 | |
| C. | 化学反应吸收或放出热量的多少与参加反应的物质的多少无关 | |
| D. | C(石墨,s)═C(金刚石,s)△H>0,所以石墨比金刚石稳定 |
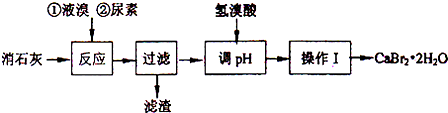
溴化钙的部分溶解度数值如下:
| 温度 | 0℃ | 10℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
| 溶解度(g) | 125 | 132 | 143 | 213 | 278 | 295 | 312 |
(2)过滤所需的玻璃仪器有玻璃棒、烧杯、漏斗.
(3)加入氢溴酸调pH的作用是除去过量的氢氧化钙.
(4)操作I包括蒸发浓缩、冷却结晶、过滤、冰水洗涤、干燥.
(5)“二氧化硫法”制备的氢溴酸粗品中常含有少量的溴和硫酸;请选用所提供的试剂,试写出检验氢溴酸粗品中是否含有SO42-的实验方案:取少量氢溴酸粗产品与试管中,滴加少量稀盐酸,再加入BaCl2溶液,若产生白色沉淀,说明含有SO42-;否则不含SO42-.
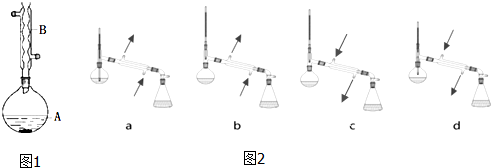
 如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对右试管小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.
如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对右试管小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.