题目内容
下列叙述不正确的是( )
| A、在熔融状态下或水溶液中均不导电的化合物,叫做非电解质 |
| B、电解质,非电解质只对化合物而言,单质不在此范畴. |
| C、易溶于水的物质一定是电解质 |
| D、硫酸铜溶液不是电解质 |
考点:电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:在熔融状态下或水溶液中均不导电的化合物,叫做非电解质;
在熔融状态下或水溶液中导电的化合物,叫做电解质;电解质的强弱与溶解性无必然联系;
单质和混合物既不是电解质也不是非电解质.
在熔融状态下或水溶液中导电的化合物,叫做电解质;电解质的强弱与溶解性无必然联系;
单质和混合物既不是电解质也不是非电解质.
解答:
解:A.在熔融状态下或水溶液中均不导电的化合物,叫做非电解质,故A正确;
B.电解质,非电解质只对化合物而言,单质既不是电解质也不是非电解质,故B正确;
C.电解质的强弱与溶解性无必然联系,乙醇易溶于水,是非电解质,故C错误;
D.硫酸铜溶液是混合物,不是电解质,故D正确;
故选C.
B.电解质,非电解质只对化合物而言,单质既不是电解质也不是非电解质,故B正确;
C.电解质的强弱与溶解性无必然联系,乙醇易溶于水,是非电解质,故C错误;
D.硫酸铜溶液是混合物,不是电解质,故D正确;
故选C.
点评:本题考查了电解质和非电解质,根据概念要点解答即可,难度不大.

练习册系列答案
相关题目
下列各组中两种元素金属性或非金属性的强弱比较正确是( )
| A、金属性:Na大于K |
| B、金属性:B大于Al |
| C、非金属性:P小于Cl |
| D、非金属性:S大于Cl |
下列叙述正确的是( )
| A、pH=5的CH3COOH溶液和pH=5的NH4NO3溶液中,c(H+)相等 |
| B、常温下1L 0.1mol/L NH4Cl溶液与2L 0.05mol/L NH4Cl溶液中C(NH4+)相等 |
| C、pH=6的CH3COOH和CH3COONa混合液中:c(Na+)+c(OH-)-c(CH3COO-)=10-6mol/L |
| D、pH=9的NaHA溶液中:c(Na+)>c(HX-)>c(A2-)>c(H2A)>c(OH-)>c(H+) |
下列离子方程式不正确的是( )
| A、向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-反应完全:NH4++2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+Al(OH)3↓+NH3?H2O |
| B、误将洁厕灵和“84”消毒液混合:2H++Cl-+ClO-═Cl2↑+H2O |
| C、向明矾溶液中加入少量的Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ |
| D、在复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能发生的离子方程式是:3NH4++Fe3++3SO42-+3Ba2++6OH-═3BaSO4↓+Fe(OH)3↓+3NH3?H2O |
在反应8P+3KOH+9H2O=3KH2PO4+5PH3中,氧化剂与还原剂的质量比为( )
| A、8:3 | B、3:8 |
| C、3:5 | D、5:3 |
1.0mol?L-1的NaCl溶液表示( )
| A、溶液中含有1mol NaCl |
| B、1mol NaCl 溶于1L水中 |
| C、58.5g NaCl溶于941.5g水中 |
| D、1L溶液里含有NaCl 58.5g |
下列说法正确的是( )
| A、乙炔的结构简式为CHCH |
| B、羟基(一OH)和氢氧根(OH一)的电子数不同 |
C、对甲基苯甲醛的结构简式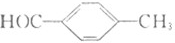 |
D、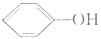 与 与 互为同系物 互为同系物 |
 某校化学实验小组同学进行有关NO2气体的系列实验.
某校化学实验小组同学进行有关NO2气体的系列实验.