题目内容
 某校化学实验小组同学进行有关NO2气体的系列实验.
某校化学实验小组同学进行有关NO2气体的系列实验.(1)如图所示,烧瓶中放有少量铜片,打开分液漏斗的旋塞,加入过量浓硝酸,烧瓶中产生气体的颜色是
(2)将烧瓶浸入冰水中,烧瓶内气体颜色
考点:氮的氧化物的性质及其对环境的影响,实验装置综合
专题:氮族元素
分析:(1)金属铜可以和浓硝酸之间反应生成硝酸铜、二氧化氮以及水,二氧化氮和水之间反应生成硝酸和一氧化氮,据此判断仪器中的颜色;
(2)二氧化氮和四氧化二氮之间存在平衡转化2NO2?N2O4.
(2)二氧化氮和四氧化二氮之间存在平衡转化2NO2?N2O4.
解答:
解:(1)金属铜可以和浓硝酸之间反应生成硝酸铜、二氧化氮以及水,即Cu+4H++NO3-=Cu2++NO2↑+4H2O,如果用水收集,则二氧化氮和水之间反应生成硝酸和一氧化氮,3NO2+H2O=2HNO3+NO,一氧化氮是无色气体,
故答案为:红棕色;无色;3NO2+H2O=2HNO3+NO;
(2)二氧化氮和四氧化二氮之间存在平衡转化:2NO2?N2O4,二氧化氮是红棕色物质,四氧化二氮是无色的,所以颜色会变浅,故答案为:变浅;
故答案为:红棕色;无色;3NO2+H2O=2HNO3+NO;
(2)二氧化氮和四氧化二氮之间存在平衡转化:2NO2?N2O4,二氧化氮是红棕色物质,四氧化二氮是无色的,所以颜色会变浅,故答案为:变浅;
点评:本题考查学生含氮化合物的性质,注意知识的迁移和应用是解题关键,难度不大.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
氯气、溴蒸气分别与氢气反应的热化学方程式如下:
H2(g)+Cl2(g)═2HCl(g)△H1=-Q1kJ/mol
H2(g)+Br2(g)═2HBr(g)△H2=-Q2kJ/mol
已知Q1>Q2>0.
下列说法正确的是( )
H2(g)+Cl2(g)═2HCl(g)△H1=-Q1kJ/mol
H2(g)+Br2(g)═2HBr(g)△H2=-Q2kJ/mol
已知Q1>Q2>0.
下列说法正确的是( )
| A、上述两个反应中反应物的总能量均大于生成物的总能量 |
| B、上述两个反应中反应物的总能量均小于生成物的总能量 |
| C、H2(g)和Cl2(g)反应生成1 mol HCl(g)时放出Q1kJ的热量 |
| D、1molHBr(g)具有的能量大于1molHBr(l)具有的能量 |
下列有机物命名正确的是( )
| A、2-乙基戊烷 |
| B、3.3-二甲基丁烷 |
| C、2,2-甲基戊烷 |
| D、间-二甲苯 |
下列叙述不正确的是( )
| A、在熔融状态下或水溶液中均不导电的化合物,叫做非电解质 |
| B、电解质,非电解质只对化合物而言,单质不在此范畴. |
| C、易溶于水的物质一定是电解质 |
| D、硫酸铜溶液不是电解质 |
锌和铝都是活泼金属,其氢氧化物均能溶于强酸,又能溶于强碱.但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成配合物离子(Zn(NH3)4)2+,除去Al3+中的杂质Zn2+,最好的方法是( )
| A、加入适量的NaOH溶液,过滤洗涤,再加盐酸 |
| B、加入过量的NaOH,过滤洗涤,再加盐酸 |
| C、加入适量的盐酸溶液,过滤洗涤再加NaOH溶液 |
| D、加入过量的氨水,过滤洗涤,再加盐酸 |
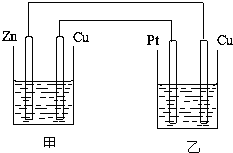 如图所示的装置,甲装置中的电解质溶液为硫酸铜溶液,乙中为稀硫酸,请按以下要求回答问题.
如图所示的装置,甲装置中的电解质溶液为硫酸铜溶液,乙中为稀硫酸,请按以下要求回答问题.