��Ŀ����
11��ͼ1�Dz��ֶ�����Ԫ�صij������ϼ���ԭ�������Ĺ�ϵͼ��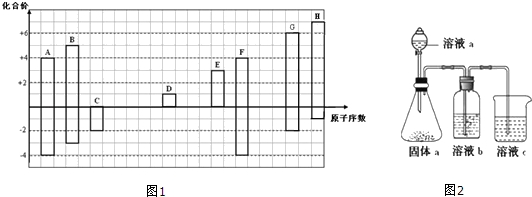
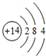
��1������Ԫ��F��ԭ�ӽṹʾ��ͼ
 ��
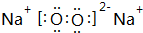
����2��������Ԫ����ѡȡ����Ԫ���γɼȺ����Ӽ��ֺ����ۼ��Ļ�����û�����ĵ���ʽΪ
 ��
����3����ЩԪ���У�����������Ӧ��ˮ������������ǿ�Ļ��������ʽΪHClO4��
��4��C��D��G��Ӧ�ļ����Ӱ뾶��С�����˳����Na+��O2-��S2-���������ӷ��Żش�
��5��ijͬѧ���ʵ��װ����ͼ2��֤��A��B��F�ķǽ�����ǿ����ϵ��
����Һa����Һb�ֱ�Ϊ���ᣬ����NaHCO3��Һ��
����Һc�е����ӷ�Ӧ����ʽΪSiO32-+CO2+H2O=H2SiO3��+CO32-��
�����ԭ�ӽṹ�ĽǶȽ��ͷǽ�����B��A��ԭ��̼�͵�Ԫ�ش���ͬһ���ڣ���ԭ�ӵĺ˵��������̼ԭ�ӣ�ԭ�Ӱ뾶��̼ԭ��С����ԭ�Ӻ˶��������ӵ����������õ���������ǿ
��6����1mol D2C2Ͷ��200mL 3mol/L EH3��Һ�У�
��ת�Ƶ��ӵ����ʵ���Ϊ1mol��
����һ����ѧ��Ӧ����ʽ��ʾ�÷�Ӧ10Na2O2+6H2O+6AlCl3=2NaAlO2+4Al��OH��3��+18NaCl+5O2 ��
���� ������Ԫ���У�A��F����+4��-4�ۣ����ڢ�A�壬��ԭ������A��F����AΪ̼��FΪSi��C��G����-2�ۣ���G��+6��G��ԭ�������ϴ�CΪOԪ�ء�GΪSԪ�أ�B��+5��-3�ۣ�ԭ����������̼����֮�䣬��BΪNԪ�أ�H��+7��-1�ۣ�ԭ��������������HΪCl��D��+1�ۣ�E��+3�ۣ��ֱ��ڢ�A�塢��A�壬ԭ������������D��E��Si����DΪNa��EΪAl��
��1��Siԭ�Ӻ��������Ϊ14����3�����Ӳ㣬���������Ϊ2��8��4��
��2������Ԫ���γɼȺ����Ӽ��ֺ����ۼ��Ļ�����ΪNa2O2�ȣ�
��3����ЩԪ���У�����������Ӧ��ˮ������������ǿ�Ļ�����Ϊ�����
��4�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵĵ��Ӳ�Խ�����Ӱ뾶Խ��
��5����װ��ͼ��֪��ʵ��ԭ��������ǿ���Ʊ����ᣬ�����ӷ���Ϊ��ֹ����Ӧ��ȥ������ƿ�в���������̼��ӦΪ������̼���η�Ӧ����Һb���ջӷ������ᣬӦΪ���͵�̼�����ƣ��ձ���Ӧ�Ƕ�����̼������Ʒ�Ӧ���ɹ��
��6���ٷ�Ӧ�й�������������������ԭ�����ã���ռһ�룬���OԪ�ػ��ϼ۱仯����ת�Ƶ��ӣ�
�ڽ�1mol Na2O2Ͷ��200mL 3mol/L AlCl3��Һ�У�����2mol NaOH��0.5mol������AlCl3�ܵ����ʵ���Ϊ0.2L��3mol/L=0.6mol��1��4��n��AlCl3����n��NaOH��=3��10��1��3��������Al��OH��3��NaAlO2����Һ������Ϊƫ�����ơ��Ȼ��ƣ����ݵ���غ����n��AlO2-������n��AlO2-��=n��NaAlO2��������AlԪ���غ����n[Al��OH��3]������ȷ��n[Al��OH��3]��n��NaAlO2����n��������������ƽ��д��
��� �⣺������Ԫ���У�A��F����+4��-4�ۣ����ڢ�A�壬��ԭ������A��F����AΪ̼��FΪSi��C��G����-2�ۣ���G��+6��G��ԭ�������ϴ�CΪOԪ�ء�GΪSԪ�أ�B��+5��-3�ۣ�ԭ����������̼����֮�䣬��BΪNԪ�أ�H��+7��-1�ۣ�ԭ��������������HΪCl��D��+1�ۣ�E��+3�ۣ��ֱ��ڢ�A�塢��A�壬ԭ������������D��E��Si����DΪNa��EΪAl��
��1��Siԭ�Ӻ��������Ϊ14����3�����Ӳ㣬���������Ϊ2��8��4��ԭ�ӽṹʾ��ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
��2������Ԫ���γɼȺ����Ӽ��ֺ����ۼ��Ļ�����ΪNa2O2�ȣ��������Ƶĵ���ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��3����ЩԪ���У�����������Ӧ��ˮ������������ǿ�Ļ�����ΪHClO4��
�ʴ�Ϊ��HClO4��
��4�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵĵ��Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶��Na+��O2-��S2-��
�ʴ�Ϊ��Na+��O2-��S2-��
��5����װ��ͼ��֪��ʵ��ԭ��������ǿ���Ʊ����ᣬ�����ӷ���Ϊ��ֹ����Ӧ��ȥ������ƿ�в���������̼��ӦΪ������̼���η�Ӧ����Һb���ջӷ������ᣬӦΪ���͵�̼�����ƣ��ձ���Ӧ�Ƕ�����̼������Ʒ�Ӧ���ɹ��ᣬ
��������������֪����ҺaΪ���ᣬ��ҺbΪ����NaHCO3��Һ���ʴ�Ϊ���������NaHCO3��Һ��
����Һc�е����ӷ���ʽΪ��SiO32-+CO2+H2O=H2SiO3��+CO32-���ʴ�Ϊ��SiO32-+CO2+H2O=H2SiO3��+CO32-��
��̼�͵�Ԫ�ش���ͬһ���ڣ���ԭ�ӵĺ˵��������̼ԭ�ӣ�ԭ�Ӱ뾶��̼ԭ��С����ԭ�Ӻ˶��������ӵ����������õ���������ǿ����˵�Ԫ�صķǽ�����ǿ��̼Ԫ�أ�
�ʴ�Ϊ��̼�͵�Ԫ�ش���ͬһ���ڣ���ԭ�ӵĺ˵��������̼ԭ�ӣ�ԭ�Ӱ뾶��̼ԭ��С����ԭ�Ӻ˶��������ӵ����������õ���������ǿ��
��6����Na2O2Ͷ AlCl3��Һ�У�����ˮ����������������������Ӧ�й�������������������ԭ�����ã���ռһ�룬��ԭ���Ĺ���������OԪ�ػ��ϼ���-1����Ϊ0�ۣ���1molNa2O2����ת�Ƶ���Ϊ1mol��$\frac{1}{2}$��2��[0-��-1��]=1mol��
�ʴ�Ϊ��1mol��
�ڽ�1mol Na2O2Ͷ��200mL 3mol/L AlCl3��Һ�У�����2mol NaOH��0.5mol������AlCl3�ܵ����ʵ���Ϊ0.2L��3mol/L=0.6mol��1��4��n��AlCl3����n��NaOH��=3��10��1��3��������Al��OH��3��NaAlO2����Һ������Ϊƫ�����ơ��Ȼ��ƣ����ݵ���غ��֪��Ӧ��n��AlO2-��=2mol-0.6mol��3=0.2mol����n��AlO2-��=n��NaAlO2��=0.2mol������AlԪ���غ��֪��n[Al��OH��3]=0.6mol-0.2mol=0.4mol����n[Al��OH��3]��n��NaAlO2����n��������=0.4mol��0.2mol��0.5mol=4��2��5����Ӧ����ʽΪ��10Na2O2+6H2O+6AlCl3=2NaAlO2+4Al��OH��3��+18NaCl+5O2 ��
�ʴ�Ϊ��10Na2O2+6H2O+6AlCl3=2NaAlO2+4Al��OH��3��+18NaCl+5O2 ��
���� ���⿼��ṹ����λ�ù�ϵ���뾶�Ƚϡ�����ʽ����ѧʵ�顢������ԭ��Ӧ���㡢����ʽ����д�ȣ��Ѷ��еȣ���6���з���ʽ��д�ؼ���ȷ������������ƫ�����ƵĹ�ϵ��Ҳ�����÷���ʽ���й���������

 ��У����ϵ�д�
��У����ϵ�д�| A�� | ������ͨ������������Һ�У�Cl2+2 OH-=H2O+Cl-+ClO- | |
| B�� | �������ڴ��CaCO3+2H+=Ca2++CO2��+H2O | |
| C�� | ����FeCl3��Һ��Ӧ��Fe+Fe3+=2Fe2+ | |
| D�� | ������Һ������������Һ��ϣ�Ba2++OH -+H++SO42-=BaSO4��+H2O |
| ѡ�� | ���ʣ�������Ϊ���ʣ� | �����Լ� |
| A | CO��CO2�� | ͨ���������ʯ��ˮ |
| B | CaCl2��Һ��HCl�� | ������Ba��OH��2��Һ |
| C | HNO3��Һ��H2SO4�� | ������BaCl2��Һ������ |
| D | NaOH��Һ��Na2CO3�� | ������Ca��OH��2��Ba��OH��2��Һ������ |
| A�� | �ֻ����õ�����ӵ�����ڶ��ε�� | |
| B�� | ͭ-п-ϡ�����ع���ʱ����ת��2mol����ʱ������������������2.24L | |
| C�� | ����ȼ�ϵ�ؿɰѻ�ѧ��תΪ���� | |
| D�� | п�̵�ء����ӵ�ء���ѧ�������ɻ�����Ⱦ��������ȼ�ϵ���ǶԻ����Ѻõĵ�� |
| A�� | ���뾶��С��S2-��Cl-��Na+��Al3+��F- | |
| B�� | ���ȶ��Դ�С��SiH4��PH3��NH3 | |
| C�� | ��ͬ��������ˮ��Ӧ�ľ��ҳ̶ȣ�Rb��K��Na��Li | |
| D�� | ����ǿ��˳��HClO4��H2SO4��H3PO4��H2SiO3 |
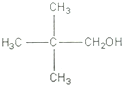
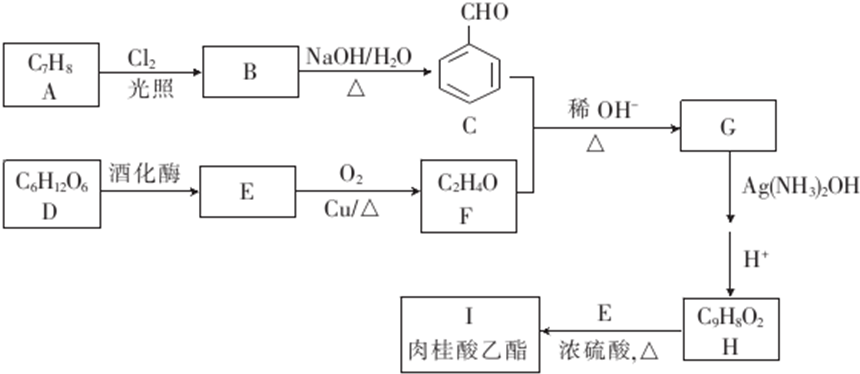
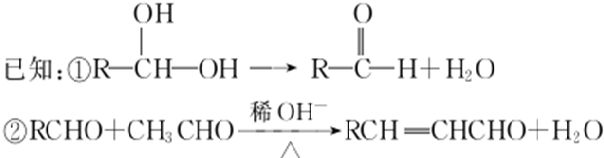
 ��E��F�ķ�Ӧ������������Ӧ��
��E��F�ķ�Ӧ������������Ӧ�� ��
��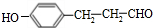 ��
��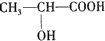 ��
��