题目内容
3.下列有关电池的说法不正确的是( )| A. | 手机上用的锂离子电池属于二次电池 | |
| B. | 铜-锌-稀硫酸电池工作时,当转移2mol电子时,正极区可生成氢气2.24L | |
| C. | 氢氧燃料电池可把化学能转为电能 | |
| D. | 锌锰电池、镍镉电池、化学电池易造成环境污染,而氢氧燃料电池是对环境友好的电池 |
分析 A.锂离子电池能反复充放电;
B.没有说明是否在标准状况下,无法计算气体的体积;
C.氢氧燃料电池属于原电池;
D.氢氧燃料电池的反应产物是水.
解答 解:A.锂离子电池能反复充放电,能循环使用,属于二次电池,故A正确;
B.没有说明是否在标准状况下,无法计算气体的体积,铜-锌-稀硫酸电池工作时,当转移2mol电子时,正极区可生成氢气0.1mol,其体积无法计算,故B错误;
C.燃料电池属于原电池,是将化学能转变为电能的装置,故C正确;
D.氢氧燃料电池的反应产物是水,对环境无污染,是对环境友好的电池,锌锰电池、镍镉电池、化学电池都含有重金属离子易造成环境污染,故D正确;
故选B.
点评 本题考查了原电池原理,根据得失电子确定正负极,再结合电极方程式中电子与物质之间的关系、原电池概念等知识点分析解答,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
18. 乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
【观察与思考】
(1)乙醇分子的核磁共振氢谱有3个吸收峰.
【活动与探究】
(2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现象.请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满).
(3)乙同学向试管中加入3~4mL无水乙醇,浸入50℃左右的热水中,再将铜丝烧至红热,迅速插入乙醇中,反复多次.则此时乙醇发生反应的化学方程式为(生成乙醛)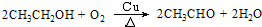 .欲验证此实验的有机产物,可以将产物加入盛有新制的氢氧化铜的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O.
.欲验证此实验的有机产物,可以将产物加入盛有新制的氢氧化铜的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O.
【交流与讨论】
(4)丙同学向一支试管中加入3mL 乙醇,然后边摇动试管边慢慢加入2mL浓硫酸和2mL冰醋酸,按右图所示连接好装置,请指出该装置的主要错误是导管插入到饱和碳酸钠溶液中.假如乙醇分子中的氧原子为18O原子,则发生此反应后
18O原子将出现在生成物B中(填字母).
A.水 B.乙酸乙酯 C.水和乙酸乙酯.
 乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.【观察与思考】
(1)乙醇分子的核磁共振氢谱有3个吸收峰.
【活动与探究】
(2)甲同学向小烧杯中加入无水乙醇,再放入一小块金属钠(约绿豆粒大),观察实验现象.请在下表中将观察到的实验现象及结论补充完全(有多少现象等就填多少,不必填满).
| 实验现象 | 结 论 | |
| ① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
| ② |
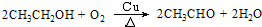 .欲验证此实验的有机产物,可以将产物加入盛有新制的氢氧化铜的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O.
.欲验证此实验的有机产物,可以将产物加入盛有新制的氢氧化铜的试管中并在酒精灯火焰上直接加热,观察现象即可,此反应的化学方程式为CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O.【交流与讨论】
(4)丙同学向一支试管中加入3mL 乙醇,然后边摇动试管边慢慢加入2mL浓硫酸和2mL冰醋酸,按右图所示连接好装置,请指出该装置的主要错误是导管插入到饱和碳酸钠溶液中.假如乙醇分子中的氧原子为18O原子,则发生此反应后
18O原子将出现在生成物B中(填字母).
A.水 B.乙酸乙酯 C.水和乙酸乙酯.
14.草酸二酯(CPPO)结构简式如右图,下列说法正确的是( )


| A. | 草酸二酯的分子式为C26H22Cl6O8 | |
| B. | 1mol草酸二酯与氢氧化钠稀溶液反应时(苯环上卤素不水解),最多消耗6mol NaOH | |
| C. | 草酸二酯酸性条件下水解可以得到两种有机物 | |
| D. | 1mol草酸二酯与氢气完全反应,需要氢气10mol |
18.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,1L C2H5OH完全燃烧后生成的CO2分子个数约为NA/11.2 | |
| B. | 18g 50%的遮糖水溶液中原子总数约为1.6 NA | |
| C. | 0℃、101KPa下,4.48LNH3中共用电子对数为0.6NA | |
| D. | 将lmol Cl2通入水中,HClO、Cl-、ClO- 粒子数之和为2NA |
8.下列鉴别方法不可行的是( )
| A. | 用水鉴别乙醇、苯和四氯化碳 | |
| B. | 用酸性高锰酸钾溶液鉴别苯、己烯和己烷 | |
| C. | 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| D. | 用燃烧法鉴别甲烷、乙烯和乙炔 |
15.下列叙述正确的是( )
| A. | 1 mol氢为2 g | B. | H2O的摩尔质量为18 g | ||
| C. | 44 g CO2的体积为22.4 L | D. | 9.8 g H2SO4含0.1NA个H2SO4分子 |
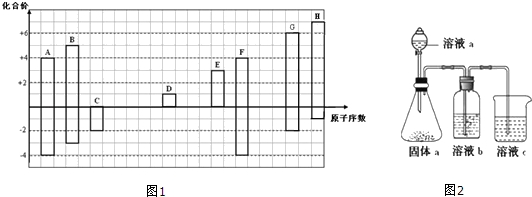
12.下列关于物质性质变化的比较,不正确的是( )
| A. | 酸性强弱:HClO4>H3PO4>H2SO4 | B. | 原子半径大小:Na>P>N | ||
| C. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3 | D. | 金属性强弱:K>Na>Li |
13.下列关于氧化还原反应的叙述中正确的是( )
| A. | 失去电子的反应为还原反应 | |
| B. | 含有氧元素的物质是氧化剂 | |
| C. | 氧化剂得到电子的数目和还原剂失去的电子的数目一定相等 | |
| D. | 氧化剂和还原剂不可能是同一种物质 |
 .
. .
.