题目内容
1.W、X、Y、Z 4种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族.下列判断错误的是( )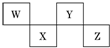
| A. | W、Y可形成两种不同的化合物 | |
| B. | Z的阴离子电子层结构与氩原子的相同 | |
| C. | W的简单氢化物的沸点比Y的氢化物的沸点高 | |
| D. | Y元素的非金属性比W元素的非金属性强 |
分析 W、X、Y、Z 4种短周期元素在元素周期表中的位置如图所示,根据元素周期表结构可知W、Y位于第二周期,X、Z位于第三周期,Z位于ⅦA族,则Z为Cl元素,故X为P元素、W为C元素、Y为O元素,据此结合元素周期律知识解答.
解答 解:W、X、Y、Z 4种短周期元素在元素周期表中的位置如图所示,根据元素周期表结构可知W、Y位于第二周期,X、Z位于第三周期,Z位于ⅦA族,则Z为Cl元素,故X为P元素、W为C元素、Y为O元素,
A.W为C元素、Y为O元素,二者可以形成二氧化碳、CO两种化合物,故A正确;
B.Z为Cl元素,氯离子核外电子总数为18,与氩原子具有相同的电子层结构,故B正确;
C.W为C,其简单氢化物为甲烷,Y为O,其氢化物为水,水分子中存在氢键,则水的沸点较高,故C错误;
D.W为C元素、Y为O元素,非金属性O>C,故D正确;
故选C.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,明确元素周期表结构为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析、理解能力及灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代得到的物质结构如图所示,对所得分子的描述,正确的是( )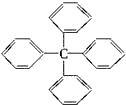

| A. | 此物质分子式为C25H18,属于苯的同系物 | |
| B. | 其一氯代物共有四种 | |
| C. | 此分子最多有13个碳原子在一个平面上 | |
| D. | 该物质能使溴水因化学反应而褪色 |
16.向10mL 0.1mol•L-1NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是( )
| A. | x=10时,溶液中有NH4+、AlO2-、SO42-,且c(NH4+)>c(SO42-) | |
| B. | x=10时,溶液中有NH4+、Al3+、SO42-,且c(NH4+)>c(Al3+) | |
| C. | x=30时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)<c(AlO2-) | |
| D. | x=30时,溶液中有Ba2+、Al3+、OH-,且c(OH-)=c(Ba2+) |
6.下列说法错误的是( )
| A. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| B. | 12g金刚石中含有的C-C键的个数为2NA | |
| C. | 配位数为4的配合物均为正四面体结构 | |
| D. | 向含有0.1mol[Co(NH3)4Cl2]Cl的水溶液中加入足量AgNO3溶液只能生成0.1molAgCl |
13.下列分离或提纯物质的方法正确的是( )
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | 硬脂酸钠 | 甘油,水 | 加NaCl | 盐析 |
| B | 乙烷 | 乙烯 | 通过KMnO4(H+)溶液 | 洗气 |
| C | C6H6 | Br2 | 加苯酚 | 过滤 |
| D | 乙酸乙酯 | 乙酸 | 氢氧化钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
10.有200mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol•L-1,c(Cl-)为1.3mol•L-1.要使Mg2+全部转化为沉淀分离出来,至少需加4mol•L-1 NaOH溶液的体积为( )
| A. | 40 mL | B. | 72 mL | C. | 80 mL | D. | 128 mL |
4.下列有机物不能使酸性高锰酸钾褪色的是( )
| A. |  | B. | 邻甲基苯酚 | C. |  | D. | 2-甲基2-己烯 |
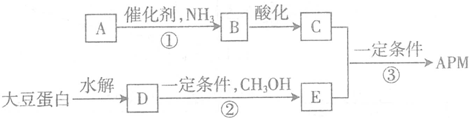
 ,C中所含官能团的名称为羧基、氨基.
,C中所含官能团的名称为羧基、氨基. .
.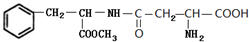 和
和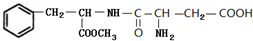 .
.