题目内容
13.下列分离或提纯物质的方法正确的是( )| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | 硬脂酸钠 | 甘油,水 | 加NaCl | 盐析 |
| B | 乙烷 | 乙烯 | 通过KMnO4(H+)溶液 | 洗气 |
| C | C6H6 | Br2 | 加苯酚 | 过滤 |
| D | 乙酸乙酯 | 乙酸 | 氢氧化钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.硬脂酸钠不溶于饱和氯化钠溶液,可用盐析的方法分离;
B.乙烯被酸性高锰酸钾氧化生成二氧化碳气体;
C.三溴苯酚与苯互溶;
D.二者都与氢氧化钠溶液反应.
解答 解:A.硬脂酸钠不溶于饱和氯化钠溶液,甘油易溶于水,可用盐析的方法分离,故A正确;
B.乙烯被酸性高锰酸钾氧化生成二氧化碳气体,引入新杂质,应用溴水除杂,故B错误;
C.三溴苯酚与苯互溶,苯不溶于水,应用氢氧化钠溶液除杂,故C错误;
D.二者都与氢氧化钠溶液反应,乙酸乙酯不溶于饱和碳酸钠溶液,可用饱和碳酸钠溶液除杂,故D错误.
故选A.
点评 本题考查混合物分离提纯方法的选择,为高频考点,把握混合物中物质的性质、性质差异为解答的关键,侧重除杂的考查,注意发生的化学反应及除杂原则,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.不久前,美国一个海军航空站安装了一台250kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600℃-700℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为2H2+O2═2H2O,负极反应为H2+CO32--2e-═H2O+CO2,则下列推断正确的是( )
| A. | 正极反应为:O2+2H2O+4e-═4OH- | |
| B. | 放电时CO32-向负极移动 | |
| C. | 电池供应1mol水蒸气,转移电子4mol | |
| D. | 放电时正极发生氧化反应 |
1.W、X、Y、Z 4种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族.下列判断错误的是( ) 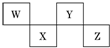

| A. | W、Y可形成两种不同的化合物 | |
| B. | Z的阴离子电子层结构与氩原子的相同 | |
| C. | W的简单氢化物的沸点比Y的氢化物的沸点高 | |
| D. | Y元素的非金属性比W元素的非金属性强 |
18.检验火柴头中含有的氯元素,先将火柴头浸没于少量水中,取其浸取液,其后的操作正确的是( )
| A. | 滴加AgNO3溶液,观察是否有白色沉淀 | |
| B. | 滴加AgNO3溶液、稀硝酸和NaNO2溶液,观察是否有白色沉淀 | |
| C. | 滴加NaOH溶液,并加热片刻,再用稀硝酸酸化后,滴入AgNO3溶液观察是否有白色沉 | |
| D. | 滴加AgNO3溶液和稀硝酸,观察是否有白色沉淀 |
5.某炔烃经催化加氢后,得到2-甲基丁烷,该炔烃是( )
| A. | 2-甲基-1-丁炔 | B. | 3-甲基-1-丁炔 | C. | 2-甲基-3-丁炔 | D. | 3-甲基-2-丁炔 |
2.下列说法正确的是(NA表示阿伏加德罗常数)( )
| A. | 0.5mol N2中含有0.5NA个N | |
| B. | 32gO2中含有的氧原子数为2NA | |
| C. | H2的摩尔质量是为2 | |
| D. | 1molH2SO4在水溶液电离出离子约为1.806×1024个 |
16.下列离子方程式正确的是( )
| A. | 铝溶于NaOH溶液:Al+2OH-=[Al(OH)4]-+H2↑ | |
| B. | 稀盐酸与铁屑反应:Fe+2H+=Fe2++H2↑ | |
| C. | 碳酸镁中滴加稀盐酸:CO32-+2H+=CO2↑+H2O | |
| D. | 稀硫酸中滴加氢氧化钡溶液:H++OH-=H2O |
 .
.