题目内容
15.17克NH3共有4mol原子,同质量的NH3和H2S分子个数比为2:1.在标准状况下,35.5g氯气的体积是11.2L,将其与氢气完全化合,需氢气的物质的量是0.5mol-1.分析 根据n=$\frac{m}{M}=\frac{N}{{N}_{A}}=\frac{V}{{V}_{m}}$结合分子的构成,以及c=$\frac{n}{V}$计算有关物理量.
解答 解:n(NH3)=$\frac{17g}{17g/mol}$=1mol,所含原子的物质的量为4mol;
由n=$\frac{m}{M}=\frac{N}{{N}_{A}}$可知:N(NH3):N(H2S)=$\frac{1}{17}:\frac{1}{34}$=2:1;
n(Cl2)=$\frac{35.5g}{71g/mol}$=0.5mol,V(Cl2)=0.5mol×22.4L/mol=11.2L;
由反应Cl2+H2=2HCl可知:需氢气的物质的量是0.5mol;
故答案为:4;2:1;11.2;0.5;
点评 本题考查物质的量的相关计算,题目难度不大,注意有关计算公式的运用.

练习册系列答案
相关题目
6.下列因果关系叙述正确的是( )
| A. | Fe3+有氧化性,实验室常用KSCN溶液检验Fe3+ | |
| B. | SO2有较强的还原性,SO2可使酸性KMnO4溶液褪色 | |
| C. | Mg有还原性,电解MgCl2饱和溶液可制备Mg | |
| D. | 浓H2SO4有吸水性,浓H2SO4可使蔗糖炭化 |
20. 已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )
已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )
 已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )
已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )| A. | T1<T2 p1>p2 m+n>p 放热反应 | B. | T1>T2 p1<p2 m+n>p 吸热反应 | ||
| C. | T1<T2 p1>p2 m+n<p 放热反应 | D. | T1>T2 p1<p2 m+n<p 吸热反应 |
7.下列物质的分类中,前者是电解质,后者是非电解质的组合是( )
| A. | NaCl、Cl2 | B. | NaHCO3、蔗糖 | C. | Ba(OH)2、HCl | D. | H2SO4、盐酸 |
5.给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
| A. | 粗硅$→_{高温}^{氯气}$ SiCl4 $→_{高温}^{氢气}$Si | |
| B. | Mg(OH)2 $\stackrel{盐酸}{→}$ MgCl2(aq)$\stackrel{电解}{→}$ Mg | |
| C. | Fe2O3 $\stackrel{盐酸}{→}$ FeCl3(aq)$\stackrel{蒸发}{→}$ 无水FeCl3 | |
| D. | AgNO3(aq)$\stackrel{NH_{3}•H_{2}O}{→}$[Ag(NH3)2]OH(aq)$→_{加热}^{蔗糖}$ Ag |


 ;E
;E .
. .
. .
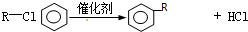
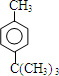
. 丙二烯(H2C=C=CH2)是重要的基础有机化学原料,可由 FeCl3 催化格氏试剂与甲基丁炔氯制备.
丙二烯(H2C=C=CH2)是重要的基础有机化学原料,可由 FeCl3 催化格氏试剂与甲基丁炔氯制备.