题目内容
13.将盐酸滴加到碳酸钙固体上,不能使反应速率加快的方法有( )| A. | 盐酸浓度不变,使用量增大1倍 | B. | 盐酸浓度增加1倍,但用量减至1/2 | ||
| C. | 将碳酸钙固体改为碳酸钙粉末 | D. | 加热此反应 |
分析 将盐酸滴加到碳酸钙固体上,能加快反应速率的方法有增大盐酸浓度、增大固体表面积、升高温度等,据此分析解答.
解答 解:A.盐酸浓度不变,使用量增大1倍,单位体积内活化分子个数不变,则反应速率不变,故A选;
B.盐酸浓度增加1倍,但用量减至1/2,增大单位体积内活化分子个数,反应速率加快,故B不选;
C.将碳酸钙固体改为碳酸钙粉末,增大反应物接触面积,反应速率加快,故C不选;
D.加热,活化分子百分数增大,反应速率加快,故D不选;
故选A.
点评 本题考查化学反应速率影响因素,为高频考点,明确浓度、温度、反应物接触面积等因素对化学反应速率影响原理是解本题关键,注意这几种外界条件适用范围,题目难度不大.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
3.下列说法错误的是( )
| A. | 金属在原电池中做正极被保护 | |
| B. | 原电池中阴离子向负极移动 | |
| C. | 常温下,强酸强碱在稀溶液中反应的中和热是-57.3KJ.mol-1 | |
| D. | 用惰性电极电解CuSO4溶液,外电路中每通过1mol电子,溶液中就产生1mol H+ |
4.H、D、T 三种同位素具有不同的( )
| A. | 质子数 | B. | 中子数 | C. | 核电荷数 | D. | 电子数 |
18.在一种酸性溶液中存在NO3-、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,由此可推知该溶液中( )
| A. | 一定含有I-,不能确定是否含有Cl- | B. | 一定含有NO3- | ||
| C. | 不含有Fe3+,可能含有NO3- | D. | 一定含有I-、NO3-和Cl- |
5.将盛有NH4HCO3的试管加热,使放出的气体依次通过盛有足量Na2O2的干燥管,足量浓H2SO4的洗气瓶,最后得到的气体( )
| A. | NH3 | B. | O2 | C. | H2O | D. | CO2 |
2.放射性同位素电池采用的放射性同位素主要有${\;}_{38}^{90}Sr$等.下列关于${\;}_{38}^{90}Sr$的说法正确的是( )
| A. | 质子数为90 | B. | 中子数为38 | C. | 电子数为52 | D. | 质量数为90 |
3.如表实验操作正确且能达到预期目的是( )
| 实验目的 | 实验操作 | |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用等量的金属钠分别与水和乙醇反应 |
| B | 检验溴乙烷中含有溴元素 | 先加NaOH溶液共热,然后加入AgNO3溶液 |
| C | 证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液 |
| D | 除去苯中的少量苯酚 | 加入过量浓溴水,振荡后过滤 |
| A. | A | B. | B | C. | C | D. | D |
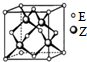 X、Y、Z、R、W、E为前四周期元素且原子序数依次增大.X的单质与Y的单质在放电条件下反应产生大气污染物,R基态原子的M能层上有3对成对电子,W核外有5个未成对电子.Y、Z分别形成氢化物Q和J,已知Q与J摩尔质量相等,Q的水溶液中加入少量WY2,立即产生大量气泡.E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
X、Y、Z、R、W、E为前四周期元素且原子序数依次增大.X的单质与Y的单质在放电条件下反应产生大气污染物,R基态原子的M能层上有3对成对电子,W核外有5个未成对电子.Y、Z分别形成氢化物Q和J,已知Q与J摩尔质量相等,Q的水溶液中加入少量WY2,立即产生大量气泡.E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题: