题目内容
3.如表实验操作正确且能达到预期目的是( )| 实验目的 | 实验操作 | |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用等量的金属钠分别与水和乙醇反应 |
| B | 检验溴乙烷中含有溴元素 | 先加NaOH溶液共热,然后加入AgNO3溶液 |
| C | 证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液 |
| D | 除去苯中的少量苯酚 | 加入过量浓溴水,振荡后过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.钠和水、乙醇反应剧烈程度不同;
B.应排除OH-离子的干扰;
C.醛基和碳碳双键都能使酸性高锰酸钾溶液氧化;
D.溴和苯酚反应生成的三溴苯酚能溶于苯中且溴单质在苯中也溶解.
解答 解:A.水中氢氧根离子和乙醇中的羟基氢活泼性不同,与钠反应剧烈程度不同,和水反应剧烈,和乙醇反应缓慢,可以利用和钠反应判断水和乙醇中羟基氢的活泼性强弱,故A正确;
B.应先加入酸中和,排除OH-离子的干扰,故B错误;
C.双键和醛基都能使高锰酸钾溶液褪色,欲证明CH2=CHCHO中含有碳碳双键需要先用新制氢氧化铜氧化醛基后再通入高锰酸钾溶液或溴水褪色证明,故C错误;
D.溴和苯酚反应生成的三溴苯酚能溶于苯中且溴单质在苯中也溶解,引入了新的杂质,故D错误.
故选A.
点评 本题考查了实验方案设计的评价,明确实验原理是解本题关键,根据物质的性质来分析解答,难度中等.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
13.将盐酸滴加到碳酸钙固体上,不能使反应速率加快的方法有( )
| A. | 盐酸浓度不变,使用量增大1倍 | B. | 盐酸浓度增加1倍,但用量减至1/2 | ||
| C. | 将碳酸钙固体改为碳酸钙粉末 | D. | 加热此反应 |
14.在8NH3+3Cl2=N2+6NH4Cl反应中,有213g氯气参加了反应,则被氧化的NH3的物质的量是( )
| A. | 2mol | B. | 3mol | C. | 1.5mol | D. | 0.2mol |
11.影响物质体积大小的因素不包括( )
| A. | 物质的粒子数目 | B. | 粒子的大小 | C. | 粒子间的距离 | D. | 粒子的运动频率 |
18.下列反应中,氧化与还原在同一元素中进行的是( )
| A. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | B. | Fe+CuSO4═FeSO4+Cu | ||
| C. | 2H2O $\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2↑ | D. | Cl2+2NaOH═NaCl+NaClO+H2O |
8.证明溴乙烷中溴原子的存在,下列正确的操作步骤为( )
①加入AgNO3溶液 ②加入NaOH水溶液 ③加热
④加入蒸馏水 ⑤加稀硝酸至溶液呈酸性 ⑥加入NaOH醇溶液.
①加入AgNO3溶液 ②加入NaOH水溶液 ③加热
④加入蒸馏水 ⑤加稀硝酸至溶液呈酸性 ⑥加入NaOH醇溶液.
| A. | ④③①⑤ | B. | ③⑥⑤① | C. | ②③① | D. | ②③⑤① |
15.下列说法中,正确的是( )
| A. | 某气体能使品红溶液褪色,则该气体是SO2 | |
| B. | 向某溶液中加入AgNO3溶液,产生白色沉淀,则原溶液中有Cl- | |
| C. | 某溶液中加入稀盐酸,不产生白色沉淀,再加入BaCl2溶液,产生白色沉淀,原溶液中有SO42- | |
| D. | 某溶液中加入盐酸产生无色气体,且该气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32-或者HCO3- |
12.针对下表中十种元素,填写空格.
(1)最不活泼的元素是Ar.
(2)S原子结构示意图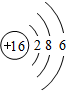 .
.
(3)N、F、Cl中,原子半径最大的是Cl.
(4)最高价氧化物对应水化物酸性最强的是高氯酸(填名称).
(5)写出实验室制氯气的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅦA | ⅧA | O |
2 | N | O | F | |||||
3 | Na | Mg | Al | S | Cl | Ar | ||
4 | K |
(2)S原子结构示意图
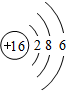 .
.(3)N、F、Cl中,原子半径最大的是Cl.
(4)最高价氧化物对应水化物酸性最强的是高氯酸(填名称).
(5)写出实验室制氯气的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.