题目内容
14.(1)BaSO4中含有少量杂质Na2SO4,为除去杂质,应从下列提供的试剂及操作方法中选择CA.加适量的稀盐酸、搅拌、蒸发、结晶 B.加适量的稀盐酸、搅拌、过滤、洗涤沉淀
C.加适量蒸馏水溶解、过滤、洗涤沉淀 D.加适量蒸馏水溶解、过滤、蒸发
(2)在漏斗中洗涤沉淀的正确操作为向漏斗中加入蒸馏水至刚好没过沉淀,让水自然流下,重复2~3次
(3)证明沉淀是否洗涤干净的操作及现象为取少量最后一次洗涤液于小试管中,滴加BaCl2溶液,如果产出白色沉淀,则没洗涤干净;反之,洗涤干净.
分析 (1)BaSO4中含有少量杂质Na2SO4,溶于水过滤即可除去;
(2)洗涤沉淀,利用过滤装置,加蒸馏水浸没沉淀;
(3)证明沉淀是否洗涤干净,检验最后一次的洗涤液是否含硫酸根离子即可.
解答 解:(1)BaSO4中含有少量杂质Na2SO4,为除去杂质,加适量蒸馏水溶解、过滤、洗涤沉淀,故答案为:C;
(2)在漏斗中洗涤沉淀的正确操作为向漏斗中加入蒸馏水至刚好没过沉淀,让水自然流下,重复2~3次,
故答案为:向漏斗中加入蒸馏水至刚好没过沉淀,让水自然流下,重复2~3次;
(3)证明沉淀是否洗涤干净的操作及现象为取少量最后一次洗涤液于小试管中,滴加BaCl2溶液,如果产出白色沉淀,则没洗涤干净;反之,洗涤干净,
故答案为:取少量最后一次洗涤液于小试管中,滴加BaCl2溶液,如果产出白色沉淀,则没洗涤干净;反之,洗涤干净.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离提纯为解答的关键,侧重分析与应用能力的考查,注意沉淀的洗涤及检验,题目难度不大.

练习册系列答案
相关题目
4. 某学生探究AgCl、Ag2S沉淀转化的原因.
某学生探究AgCl、Ag2S沉淀转化的原因.
(1)Ⅰ中的白色沉淀是AgCl.
(2)Ⅱ中能说明沉淀变黑的离子方程式是2AgCl(s)+S2-?Ag2S(s)+2Cl-,沉淀转化的主要原因是Ag2S比AgCl溶解度更小.
(3)滤出步骤Ⅲ中乳白色沉淀,推测含有AgCl.用浓HNO3溶解,产生红棕色气体,部分沉淀未溶解,过滤得到滤液X和白色沉淀Y.
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀
ⅱ.向Y滴加KI溶液,产生黄色沉淀
①由ⅰ判断,滤液X中被检出的离子是SO42-.
②由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有AgCl和另一种沉淀S.
(4)该学生通过如下对照实验确认了步骤Ⅲ中乳白色沉淀产生的原因:在NaCl存在下,氧气将Ⅲ中黑色沉淀氧化.
①A中产生的气体是O2.
②C中盛放的物质W是Ag2S的悬浊液.
③该同学认为B中产生沉淀的反应如下(请补充完整):
2Ag2S+1O2++4NaCl+2H2O?4AgCl+2S+4NaOH.
 某学生探究AgCl、Ag2S沉淀转化的原因.
某学生探究AgCl、Ag2S沉淀转化的原因.| 步 骤 | 现 象 |
| Ⅰ.将NaCl与AgNO3溶液混合 | 产生白色沉淀 |
| Ⅱ.向所得固液混合物中加Na2S溶液 | 沉淀变为黑色 |
| Ⅲ.滤出黑色沉淀,加入NaCl溶液 | 较长时间后,沉淀变为乳白色 |
(2)Ⅱ中能说明沉淀变黑的离子方程式是2AgCl(s)+S2-?Ag2S(s)+2Cl-,沉淀转化的主要原因是Ag2S比AgCl溶解度更小.
(3)滤出步骤Ⅲ中乳白色沉淀,推测含有AgCl.用浓HNO3溶解,产生红棕色气体,部分沉淀未溶解,过滤得到滤液X和白色沉淀Y.
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀
ⅱ.向Y滴加KI溶液,产生黄色沉淀
①由ⅰ判断,滤液X中被检出的离子是SO42-.
②由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有AgCl和另一种沉淀S.
(4)该学生通过如下对照实验确认了步骤Ⅲ中乳白色沉淀产生的原因:在NaCl存在下,氧气将Ⅲ中黑色沉淀氧化.
| 现象 | B.一段时间后,出现白色沉淀 |
| C.一点时间后,无明显变化 |
②C中盛放的物质W是Ag2S的悬浊液.
③该同学认为B中产生沉淀的反应如下(请补充完整):
2Ag2S+1O2++4NaCl+2H2O?4AgCl+2S+4NaOH.
5.在固定容积的容器中,某化学反应2A(g)?B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度( mol/L )随反应时间( min )的变化情况见表.
根据上述数据,完成下列填空:
(1)在实验1中,反应在10min至20min时间内平均速率v(A)为0.013mol/(L•min);达到平衡时A的转化率是50%,B的浓度是0.25mol/L;800℃时,该反应2A(g)?B(g)+D(g) 的平衡常数数值是0.25;若同温下,另一个恒容密闭的容器中也在发生该反应,某时刻A、B、D的浓度均为2mol/L,则该时刻v(正)<v(逆)(填“>”“=”或“<”).
(2)在实验2中,A的初始浓度c1=1.0mol/L,反应经20min就达到平衡,可推测实验2中还隐含的条件是使用了催化剂.
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3<v1(填“>”“=”或“<”),且c2> 1.0mol/L (填“>”“=”或“<”).
(4)比较实验4和实验1,可推测该反应是放热反应(填“吸热”或“放热”).
| 实验序号 | 温度 | 0min | 10min | 20min | 30min | 40min | 50min | 60min |
| 1 | 820℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 820℃ | c1 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c2 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 800℃ | 1.0 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验1中,反应在10min至20min时间内平均速率v(A)为0.013mol/(L•min);达到平衡时A的转化率是50%,B的浓度是0.25mol/L;800℃时,该反应2A(g)?B(g)+D(g) 的平衡常数数值是0.25;若同温下,另一个恒容密闭的容器中也在发生该反应,某时刻A、B、D的浓度均为2mol/L,则该时刻v(正)<v(逆)(填“>”“=”或“<”).
(2)在实验2中,A的初始浓度c1=1.0mol/L,反应经20min就达到平衡,可推测实验2中还隐含的条件是使用了催化剂.
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3<v1(填“>”“=”或“<”),且c2> 1.0mol/L (填“>”“=”或“<”).
(4)比较实验4和实验1,可推测该反应是放热反应(填“吸热”或“放热”).
2.要从含Al3+、Fe3+、Ba2+、Ag+的溶液中分别一一沉淀出Fe3+、Ba2+、Ag+,加入试剂的顺序正确的是( )
| A. | HCl、H2SO4、NH3•H2O | B. | NaOH、HCl、H2SO4 | ||
| C. | HCl、H2SO4、NaOH | D. | HCl、NaOH、H2SO4 |

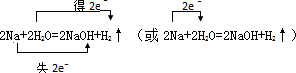 .反应中若产生0.2mol的气体,则有0.4mol的电子转移.
.反应中若产生0.2mol的气体,则有0.4mol的电子转移.