题目内容
17.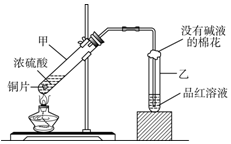 用如图所示的装置可以验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质.
用如图所示的装置可以验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质.(1)通过试管乙中发生的品红溶液褪色现象说明了铜和浓硫酸发生了化学反应,并且该现象还能说明产生的气体具有漂白性.
(2)试管乙口部浸有碱液棉花作用是吸收SO2,防止环境污染.
(3)写出试管甲中所发生反应的化学方程式Cu+2H2SO4$\frac{\underline{\;加热\;}}{\;}$CuSO4+SO2↑+2H2O.
分析 加热条件下金属铜和浓硫酸发生反应生成硫酸铜、水和二氧化硫,二氧化硫能使品红褪色,具有漂白性,二氧化硫可与氢氧化钠溶液反应,用浸有碱液棉花可防止污染空气,以此解答该题.
解答 解:(1)金属铜和浓硫酸发生反应生成硫酸铜、水和二氧化硫,生成的二氧化硫具有漂白性,能使品红褪色,故答案为:品红溶液褪色;漂白;
(2)二氧化硫有毒,能污染空气,属于酸性氧化物,能和碱反应生成盐和水,在装置口处浸有碱液的棉花可以和二氧化硫反应,
故答案为:吸收SO2,防止环境污染;
(3)金属铜和浓硫酸发生反应生成硫酸铜、水和二氧化硫,方程式为Cu+2H2SO4$\frac{\underline{\;加热\;}}{\;}$CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4$\frac{\underline{\;加热\;}}{\;}$CuSO4+SO2↑+2H2O.
点评 本题考查学生浓硫酸的性质以及二氧化硫的性质,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握浓硫酸、二氧化硫等物质的性质,难度不大.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
7.下列化合物中,在常温常压下以液态形式存在的是( )
| A. | 乙烷 | B. | 乙烯 | C. | 乙块 | D. | 甲醇 |
12.下列反应的离子方程式书写正确的是( )
| A. | Al2O3和NaOH溶液反应:Al2O3+2OH-═2AlO2-+H2↑ | |
| B. | AlCl3与过量NaOH溶液反应:Al3++3OH-═Al(OH)2↓ | |
| C. | NO2溶于水:3NO2+H2O═2NO3-+2H++NO↑ | |
| D. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ |
2.用下列实验装置完成对应实验(部分仪器已省略)不能达到实验目的是( )
| A. | 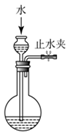 检查装置气密性 | |
| B. |  实验室制氨气 | |
| C. | 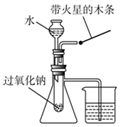 验证过氧化钠与水反应即生成氧气又放热 | |
| D. |  分离苯和水 |
9.甲、乙两烧杯中各盛有100mL3mol/L的盐酸和NaOH溶液,向两烧杯中分别加入足量的铝粉,反应结束后再同条件下测得生成的气体体积比为( )
| A. | 1:1 | B. | 1:3 | C. | 1:2 | D. | 3:1 |
6.为有效控制雾霾,各地积极采取措施改善大气质量.研究并有效控制空气中氮氧化物、碳氧化物含量显得尤为重要.
Ⅰ.氮氧化物研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应:2NO(g)+O2(g)?2NO2(g),下列各项能说明该反应达到平衡状态的是abc.
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗1molO2,同时生成2molNO2
(2)在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如图1所示,根据图象判断反应N2(g)+O2(g)?2NO(g)的△H>0(填“>”或“<”).
(3)NOx是汽车尾气中的主要污染物之一.汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图2:出该反应的热化学方程式:N2(g)+O2(g)=2NO(g)△H=+183kJ•mol-1.
Ⅱ.碳氧化物研究
(1)在体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图3所示,现将3molNH3和2molCO2放入容器中,移动活塞至体积V为2L,用铆钉固定在A、B点,发生合成尿素的总反应如下:
CO(g)+2H2(g)?CH3OH(g)
测定不同条件、不同时间段内的CO的转化率,得到如下数据:
①根据上表数据,请比较T1>T2(选填“>”、“<”或“=”);T2℃下,第30min 时,a1=50%,该温度下的化学平衡常数为4.
②T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人6molCO,此时v(正)<v (逆)(选填“>”、“<”或“=”),判断的理由是拔去铆钉,容器是在同温同压下进行,体积之比等于物质的量之比,当冲入6molCO,假设平衡不移动,此时容器的体积为6L,Qc=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$=$\frac{36}{7}$>K,故平衡逆向移动,v(正)<v(逆).
(2)一定条件下可用甲醇与CO反应生成醋酸消除CO污染.常温下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=$\frac{2b}{a-2b}×1{0}^{-7}mol/L$(用含a和b的代数式表示)
Ⅰ.氮氧化物研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应:2NO(g)+O2(g)?2NO2(g),下列各项能说明该反应达到平衡状态的是abc.
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗1molO2,同时生成2molNO2
(2)在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如图1所示,根据图象判断反应N2(g)+O2(g)?2NO(g)的△H>0(填“>”或“<”).

(3)NOx是汽车尾气中的主要污染物之一.汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图2:出该反应的热化学方程式:N2(g)+O2(g)=2NO(g)△H=+183kJ•mol-1.
Ⅱ.碳氧化物研究
(1)在体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图3所示,现将3molNH3和2molCO2放入容器中,移动活塞至体积V为2L,用铆钉固定在A、B点,发生合成尿素的总反应如下:
CO(g)+2H2(g)?CH3OH(g)
测定不同条件、不同时间段内的CO的转化率,得到如下数据:
| 10min | 20min | 30min | 40min | |
| T1 | 30% | 55% | 65% | 65% |
| T2 | 35% | 50% | a1 | a2 |
②T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人6molCO,此时v(正)<v (逆)(选填“>”、“<”或“=”),判断的理由是拔去铆钉,容器是在同温同压下进行,体积之比等于物质的量之比,当冲入6molCO,假设平衡不移动,此时容器的体积为6L,Qc=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$=$\frac{36}{7}$>K,故平衡逆向移动,v(正)<v(逆).
(2)一定条件下可用甲醇与CO反应生成醋酸消除CO污染.常温下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=$\frac{2b}{a-2b}×1{0}^{-7}mol/L$(用含a和b的代数式表示)
7.化学反应4A(s)+3B(g)?2C(g)+D(g)经2min,B的浓度减少0.6mol•L-1.对此反应速率的表示正确的是( )
| A. | 2 min内,用A表示的反应速率是0.4 mol•L-1•min-1 | |
| B. | 分别用B、C、D表示的反应速率其比值是1:1:1 | |
| C. | 2 min时间内反应速率,用B表示是0.3 mol•L-1•min-1 | |
| D. | 2 min内用C表示的反应速率v (C)是0.3 mol•L-1•min-1 |