题目内容
16.下列能产生丁达尔现象的是( )| A. | 氯化钠溶液 | B. | 氢氧化铁胶体 | C. | 盐酸 | D. | 硫酸铜溶液 |
分析 丁达尔效应是指:当一束光线透过胶体,从入射光的垂直方向可以观察到胶体里出现的一条光亮的“通路.丁达尔现象是胶体特有的性质,抓住这一特点即可解答.
解答 解:A.氯化钠溶液分散质微粒直径小于1nm是溶液,没有丁达尔效应,故A错误;
B.氢氧化铁胶体分散质微粒直径在1-100nm之间是胶体,有丁达尔效应,故B正确;
C.盐酸溶液分散质微粒直径小于1nm是溶液,没有丁达尔效应,故C错误;
D.硫酸铜溶液分散质微粒直径小于1nm是溶液,没有丁达尔效应,故D错误.
故选B.
点评 本题考查了胶体的性质应用,注意丁达尔效应是胶体特有的性质是解答本题的关键,题目难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
4.含6.02×1023个中子的${\;}_3^7Li$的质量是( )
| A. | $\frac{7}{4}g$ | B. | 4.7 g | C. | 7.4 g | D. | $\frac{4}{7}g$ |
11.化学与人类生产、生活、社会可持续发展密切相关,下列说法正确的是( )
| A. | 次氯酸具有强氧化性,可以起到除去水中悬浮的杂质和杀菌消毒作用 | |
| B. | 为防止中秋月饼等富脂食品氧化变质,常在包装中放入生石灰 | |
| C. | 金属汞一旦洒落在地面或桌面时,必须尽可能收集,并深埋处理 | |
| D. | 高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 |
8.下列各组物质中,所含原子数相等的是( )
| A. | 10g H2和10g O2 | B. | 标准状况下相同体积的N2和H2 | ||
| C. | 9g水和0.25mol H2 | D. | 22g CO2和3.01×1023个N2 |
5.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 11gT2O含有的电子数为5NA | |
| B. | 常温下,0.2L 0.5mol•L-1NH4NO3溶液的氮原子数小于0.2NA | |
| C. | 含4molHCl的浓盐酸与足量二氧化锰反应转移的电子总数为NA | |
| D. | 标准状况下,2.24L H2S全部溶于水所得溶液中HS-和S2-离子激之和为0.1NA |
6.分枝酸可用于生化研究,其结构简式为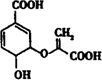 ,下列关于分枝酸的说法不正确的是( )
,下列关于分枝酸的说法不正确的是( )
 ,下列关于分枝酸的说法不正确的是( )
,下列关于分枝酸的说法不正确的是( )| A. | 分子中含有3种含氧官能团 | |
| B. | 1 mol分枝酸最多可与2mol NaOH发生中和反应 | |
| C. | 在一定条件下可与乙醇、乙酸反应,但反应类型不相同 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,但褪色原理不同 |
 如图所涉及的物质均为中学化学中的常见物质,其中C、D、E为单质,其余为化合物,F为磁性物质.它们存在如下转化关系,反应中生成的水及次要产物均已略去.
如图所涉及的物质均为中学化学中的常见物质,其中C、D、E为单质,其余为化合物,F为磁性物质.它们存在如下转化关系,反应中生成的水及次要产物均已略去.