题目内容
19.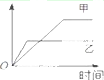 表格中的各种情况,可以用如图的曲线表示的是( )
表格中的各种情况,可以用如图的曲线表示的是( ) | 反 应 | 纵坐标 | 甲 | 乙 | |
| A | 相同质量的氨,在同一容器中 2NH3═N2+3H2 △H<0 | 氨气的转化率 | 500℃ | 400℃ |
| B | 等质量钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
| C | 向温度和压强都相同的甲乙两容器中分别投入体积比1:3的N2、H2(N2+3H2═2NH3) | 氨气的物质的量 | 反应过程中保持恒温恒容 | 反 应过程中保持恒温恒压 |
| D | 2molSO2和1molO2,在相同温度下 2SO2+O2═2SO3 | SO3 的浓度 | 2个大气压 | 10个大气压 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、温度越高化学发应速率越快;
B、根据金属钾和金属钠与水的反应进行回答;
C、恒温恒容就是在恒温恒压的条件下减小压强;
D、增大压强化学平衡向着气体体积减小的方向进行.
解答 解:A、对于反应2NH3?N2+3H2,温度越高化学发应速率越快,所以甲达到化学平衡用的时间短,故A错误;
B、根据金属钾和金属钠与水反应的原理方程式可知,2Na~H2,2K~H2,等质量钾、钠,则金属钠的物质的量大,所以金属钠产生的氢气多,金属钾的活泼性强与金属钠,所以金属钾的反应速率快,故B正确;
C、恒温恒容就是在恒温恒压的条件下减小压强,减小压强平衡逆向移动,达平衡的时间增大,而不是缩短,故C错误;
D、对于反应2SO2+O2?2SO3,增大压强化学平衡向着正反应方向进行,所以达到平衡时,乙的三氧化硫的量高于甲的,故D错误.
故选B.
点评 本题是一道图象题,注意拐点处的含义以及化学反应速率和化学平衡的影响因素知识,可以根据教材知识来回答,难度中等.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
5.甲、乙、丙三种可溶性盐,其中所含阳离子的原子序数依次增大,现将等物质的量的三种物质混合后溶于水,产生白色沉淀,溶液中还含有下列五种离子:Al3+、Na+、NO3-、Cl-、SO42-.下列有关说法不正确的是( )
| A. | 丙的阳离子可能不是主族元素 | B. | 乙可能是硝酸铝 | ||
| C. | 甲可能是硫酸钠 | D. | 所得溶液呈弱酸性 |
10.等质量的下列物质所含分子数最多的是( )
| A. | N2 | B. | HCl | C. | O2 | D. | NH3 |
7.下列做法不利于“开源节流”的是( )
| A. | 开发太阳能、水能、风能、地热等新能源 | |
| B. | 减少资源消耗,注重资源的重复使用、资源的循环再生 | |
| C. | 大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 | |
| D. | 大力开采煤、石油和天然气,以满足人们日益增长的能源需求 |
14.下列有关物质结构的说法中,正确的是( )
| A. | 用VSEPR理论预测BF3和NF3的立体构型均为平面三角形 | |
| B. | CO2是直线形分子,其中碳原子的杂化轨道类型为sp3杂化 | |
| C. | 电子层结构相同的简单离子,其半径随核电荷数增大而减小 | |
| D. | 在化学反应中,某元素由化合态变为游离态,则该元素一定被还原 |
11.分子式为C7H6O2 的芳香化合物(只有一个环),其同分异构体最多有( )种.
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
8.在电解冶炼铝的电解槽中存在电解质W2[X2Y2Z4].已知其涉及的四种元素的简单离子的电子层结构均相同,
Y原子最外层电子数为次外层的3倍,X原子最外层电子数为Y原子最外层电子数的一半.下列说法正确的是
( )
Y原子最外层电子数为次外层的3倍,X原子最外层电子数为Y原子最外层电子数的一半.下列说法正确的是
( )
| A. | 原子序数:W>X>Y>Z | B. | 原子半径:W>X>Y>Z | ||
| C. | 最高价氧化物对应的碱的碱性:W<X | D. | 最简单氧化物的稳定性:Y>Z |
9.下列有关晶体的叙述中,错误的是( )
| A. | 金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 | |
| B. | 氯化钠晶体中,每个Na+周围距离相等且最近的Na+共有6个 | |
| C. | 金属晶体中,铜和锌都是面心立方堆积 | |
| D. | 干冰晶体中,每个CO2分子周围距离相等且最近的CO2分子共有12个 |