题目内容
20.下列各组物质只用胶头滴管和试管不能鉴别的是( )| A. | KOH溶液与AlCl3溶液 | B. | NaAlO2溶液与盐酸 | ||
| C. | NaHCO3溶液与盐酸 | D. | Na2CO3溶液与盐酸 |
分析 只要用试管和胶头滴管,不用任何化学试剂就可以鉴别的物质可以采用相互滴加的方法检验,滴加顺序不同,现象不同的可以鉴别,否则不能鉴别,以此解答.
解答 解:A.将氯化铝溶液滴加到KOH溶液中先没有现象,后生成沉淀,将KOH滴到氯化铝溶液中先生成沉淀后沉淀消失,二者现象不同,可鉴别,故A不选;
B.向NaAlO2溶液加盐酸,先有沉淀后沉淀消失,而向盐酸中加NaAlO2溶液,先没有沉淀后生成沉淀,现象不同,能鉴别,故B不选;
C.无论将盐酸滴到NaHCO3溶液中还是将NaHCO3溶液滴到盐酸中都生成立即出现气泡,现象相同,不能鉴别,故C选;
D.Na2CO3溶液滴入稀盐酸中,立即产生气体,若将盐酸滴入Na2CO3溶液中,开始没有气体生成,后有气体生成,二者显现不同,可鉴别,故D不选;
故选C.
点评 本题考查利用滴加顺序不同鉴别物质,为高频考点,注意滴加顺序不同实质是反应物量的不同,掌握常见与量及顺序有关的反应,注意基础知识的全面掌握,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列认识正确的是( )
| A. | H2与D2、T2互为同位素 | |
| B. | 氯化钠溶液和氢氧化铁胶体可以用过滤的方法分离 | |
| C. | NH3溶于水可以导电,但不是电解质 | |
| D. | SO2、NO2均属于酸性氧化物 |
15.在花瓶中加入“营养液”,能延长鲜花的寿命.下表是500mL“营养液”中含有的成分,阅读后回答下列问题:
(1)下列“营养液”的成分中,属于非电解质的是A.(填序号)
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“营养液”中K+(阿司匹林中不含K+)的物质的量浓度为$\frac{\frac{0.5}{158}+\frac{0.5}{174}×2}{0.5}$ mol•L-1(只要求写表达式,不用写出计算结果).
(3)配制上述“营养液”500mL所需的仪器有:电子天平、药匙、烧杯、500ml容量瓶、玻璃棒、胶头滴管.(在横线上填写所缺仪器的名称)
(4)在配制一定物质的量浓度的溶液时,一般可分为以下几个步骤:①称量②计算③溶解
④摇匀⑤转移⑥洗涤⑦定容⑧冷却.其正确的操作顺序为②①③⑧⑤⑥⑦④.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BC,使所配制溶液的浓度偏高的是A,偏低的是DE.
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
D.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
E.定容时发现液面高于容量瓶的刻度线,倒出一部分液体后再加蒸馏水至刻度线.
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 50.0 | 342 |
| 硫酸钾 | 0.5 | 174 |
| 阿司匹林 | 0.4 | 180 |
| 高锰酸钾 | 0.5 | 158 |
| 硝酸银 | 0.2 | 170 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“营养液”中K+(阿司匹林中不含K+)的物质的量浓度为$\frac{\frac{0.5}{158}+\frac{0.5}{174}×2}{0.5}$ mol•L-1(只要求写表达式,不用写出计算结果).
(3)配制上述“营养液”500mL所需的仪器有:电子天平、药匙、烧杯、500ml容量瓶、玻璃棒、胶头滴管.(在横线上填写所缺仪器的名称)
(4)在配制一定物质的量浓度的溶液时,一般可分为以下几个步骤:①称量②计算③溶解
④摇匀⑤转移⑥洗涤⑦定容⑧冷却.其正确的操作顺序为②①③⑧⑤⑥⑦④.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BC,使所配制溶液的浓度偏高的是A,偏低的是DE.
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
D.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
E.定容时发现液面高于容量瓶的刻度线,倒出一部分液体后再加蒸馏水至刻度线.
9.下列物质中,既能与盐酸反应,又能跟NaOH溶液反应的化合物是( )
①NaHCO3 ②Al ③Al2O3 ④Al(OH)3 ⑤Na2SO4.
①NaHCO3 ②Al ③Al2O3 ④Al(OH)3 ⑤Na2SO4.
| A. | ①③④⑤ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
10.在某温度时,将nmol/L的氨水滴入10mL0.1mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示.下列有关说法正确的是( )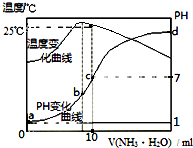

| A. | a点KW=1.0×10-14 | |
| B. | 水的电离程度:b>c>a>d | |
| C. | b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-) | |
| D. | 25℃时,一水合氨的电离平衡常数为$\frac{1{0}^{-7}}{(10n-1)}$(用n表示) |




 、
、 、
、 烯烃的名称:
烯烃的名称: