��Ŀ����
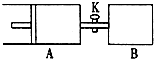 ��ͼ������A����ǿ�ƽ���ƶ��Ļ������رջ���K����A�г���1molX��1molY����B�г���2molX��2molY����ʼʱA��B�����������aL�����¶���ͬ�����ѹǿ��ͬ�ʹ������ڵ������£�ʹ���������Է�����Ӧ��X��g��+Y��g��?Z��g��+2W��g������ƽ��ʱ��A�����Ϊ1.2aL������˵����ȷ���ǣ�������
��ͼ������A����ǿ�ƽ���ƶ��Ļ������رջ���K����A�г���1molX��1molY����B�г���2molX��2molY����ʼʱA��B�����������aL�����¶���ͬ�����ѹǿ��ͬ�ʹ������ڵ������£�ʹ���������Է�����Ӧ��X��g��+Y��g��?Z��g��+2W��g������ƽ��ʱ��A�����Ϊ1.2aL������˵����ȷ���ǣ�������| A����Ӧ���ʣ�V��B����V��A�� |
| B��A������Xת����Ϊ20% |
| C��ƽ��ʱ��ѹǿ��P��B��=2P��A�� |
| D������K����ﵽ�µĻ�ѧƽ��ʱ��A�����Ϊ2.6aL |
���㣺��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
������A��������A��˵���ڽ�����ѧƽ��Ĺ����У���Ӧ�����������ʵ����������ݰ���٤�����ɣ�ͬ��ͬ��ʱ��ѹǿ֮�ȵ������ʵ���֮�ȣ��������Ҫ������ֵ����ʵ���Ũ�Ⱦ�Ҫ���£��䷴Ӧ����ҲҪ��С������B������˵��������䣬����ֳ�ʼŨ����A������2����ÿ��ʱ�̵ķ�Ӧ���ʶ�������A����������Ӧ���ʣ�v��B����v��A����
B�����ݰ���٤�����ɣ�ͬ��ͬ��ʱ��ѹǿ֮�ȵ������ʵ���֮�ȣ���ƽ������������ʵ����dz�ʼʱ���ʵ�����1.2������1.2��2mol=2.4mol����������0.4mol�����ݻ�ѧ����ʽ�ļ��������
C����ΪB�����ij�ʼ����A������2��������ͬ�¶��£���A�����������B��������Ķ���֮һ����0.5aL��ʱ���ﵽƽ�����ֵ�Ũ�ȡ��ٷֺ�����������ѹǿ����ȣ���ѹǿΪPB�����Ѵ�ʱA���������0.5a�������Ϊ1.4aL��������ƽ���ƶ�ʱѹǿ���Ϊ
�����ٽ���ƽ��ʱ��A������ԭƽ�⽫������Ӧ�����ƶ�����������������ʵ���Ҫ���ӣ�������仯��ѹǿ��Ӱ���
D������K���൱�ڵ�ѹ����ԭ����A��Ч���ʷ�Ӧ��������Ϊ1.2a��3=3.6a��������ﵽ�µĻ�ѧƽ��ʱ��A�����Ϊ2.6aL��
B�����ݰ���٤�����ɣ�ͬ��ͬ��ʱ��ѹǿ֮�ȵ������ʵ���֮�ȣ���ƽ������������ʵ����dz�ʼʱ���ʵ�����1.2������1.2��2mol=2.4mol����������0.4mol�����ݻ�ѧ����ʽ�ļ��������
C����ΪB�����ij�ʼ����A������2��������ͬ�¶��£���A�����������B��������Ķ���֮һ����0.5aL��ʱ���ﵽƽ�����ֵ�Ũ�ȡ��ٷֺ�����������ѹǿ����ȣ���ѹǿΪPB�����Ѵ�ʱA���������0.5a�������Ϊ1.4aL��������ƽ���ƶ�ʱѹǿ���Ϊ
| 5P B |
| 14 |
D������K���൱�ڵ�ѹ����ԭ����A��Ч���ʷ�Ӧ��������Ϊ1.2a��3=3.6a��������ﵽ�µĻ�ѧƽ��ʱ��A�����Ϊ2.6aL��
���
�⣺A����X��g��+Y��g��?2Z��g��+W��g����˵����ʼʱֻ���뷴Ӧ��X��Y���÷�Ӧ��������Ӧ��������Խ�����ѧƽ�⣮������A��˵���ڽ�����ѧƽ��Ĺ����У���Ӧ�����������ʵ����������ݰ���٤�����ɣ�ͬ��ͬ��ʱ��ѹǿ֮�ȵ������ʵ���֮�ȣ��������Ҫ������ֵ����ʵ���Ũ�Ⱦ�Ҫ���£��䷴Ӧ����ҲҪ��С������B������˵��������䣬����ֳ�ʼŨ����A������2����ÿ��ʱ�̵ķ�Ӧ���ʶ�������A����������Ӧ���ʣ�v��B����v��A������A����
B�����ݰ���٤�����ɣ�ͬ��ͬ��ʱ��ѹǿ֮�ȵ������ʵ���֮�ȣ�����ƽ������������ʵ����dz�ʼʱ���ʵ�����1.2������1.2��2mol=2.4mol����������0.4mol�����ݻ�ѧ����ʽ�ļ����֪��
X ��g��+Y��g��?Z��g��+2W��g����n
1 1
0.4mol 0.4mol
����ƽ���Ӧ��0.4mol��A������X��ת����Ϊ40%����B����
C����ΪB�����ij�ʼ����A������2��������ͬ�¶��£���A�����������B��������Ķ���֮һ����0.5aL��ʱ���ﵽƽ�����ֵ�Ũ�ȡ��ٷֺ�����������ѹǿ����ȣ���ѹǿΪPB�����Ѵ�ʱA���������0.5a�������Ϊ1.4aL��������ƽ���ƶ�ʱѹǿ���Ϊ5PB/14�����ٽ���ƽ��ʱ��A������ԭƽ�⽫������Ӧ�����ƶ�����������������ʵ���Ҫ���ӣ�������仯��ѹǿ��Ӱ���PB��2PA����C����
D������K���൱�ڵ�ѹ����ԭ����A��Ч���ʷ�Ӧ��������Ϊ1.2a��3=3.6a��������ﵽ�µĻ�ѧƽ��ʱ��A�����Ϊ2.6aL����D��ȷ��
��ѡD��
B�����ݰ���٤�����ɣ�ͬ��ͬ��ʱ��ѹǿ֮�ȵ������ʵ���֮�ȣ�����ƽ������������ʵ����dz�ʼʱ���ʵ�����1.2������1.2��2mol=2.4mol����������0.4mol�����ݻ�ѧ����ʽ�ļ����֪��
X ��g��+Y��g��?Z��g��+2W��g����n
1 1
0.4mol 0.4mol
����ƽ���Ӧ��0.4mol��A������X��ת����Ϊ40%����B����
C����ΪB�����ij�ʼ����A������2��������ͬ�¶��£���A�����������B��������Ķ���֮һ����0.5aL��ʱ���ﵽƽ�����ֵ�Ũ�ȡ��ٷֺ�����������ѹǿ����ȣ���ѹǿΪPB�����Ѵ�ʱA���������0.5a�������Ϊ1.4aL��������ƽ���ƶ�ʱѹǿ���Ϊ5PB/14�����ٽ���ƽ��ʱ��A������ԭƽ�⽫������Ӧ�����ƶ�����������������ʵ���Ҫ���ӣ�������仯��ѹǿ��Ӱ���PB��2PA����C����
D������K���൱�ڵ�ѹ����ԭ����A��Ч���ʷ�Ӧ��������Ϊ1.2a��3=3.6a��������ﵽ�µĻ�ѧƽ��ʱ��A�����Ϊ2.6aL����D��ȷ��
��ѡD��
�����������ѶȽϴ���Ҫ���ƽ��ͱ任ƽ�⣬Ҫ����������˼ά���̣���һ��ѵ��˼ά�ĺ��⣮

��ϰ��ϵ�д�
�����Ŀ
��ҩݭ�������к���һ��ɫ�أ����Ľṹ��ͼ����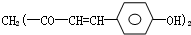 ���Ƴɵ���ֽ���Լ�������ԣ��ܹ���1mol�û�������Ӧ��NaOH��H2��������ֱ�Ϊ��������
���Ƴɵ���ֽ���Լ�������ԣ��ܹ���1mol�û�������Ӧ��NaOH��H2��������ֱ�Ϊ��������
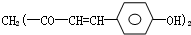 ���Ƴɵ���ֽ���Լ�������ԣ��ܹ���1mol�û�������Ӧ��NaOH��H2��������ֱ�Ϊ��������
���Ƴɵ���ֽ���Լ�������ԣ��ܹ���1mol�û�������Ӧ��NaOH��H2��������ֱ�Ϊ��������| A��3mol��3mol |
| B��1mol��5mol |
| C��6mol��8mol |
| D��2mol��10mol |
��һ�ܱ������У��õ����ʵ�����A��B�������·�Ӧ��A������+2B������?2C��������Ӧ��5min ʱ��A��ת����Ϊ0.4�����ʱ����������ʵ���n��A����n��B����n��C��Ӧ����Ĺ�ϵ�ǣ�������
| A��n��A��=n��C�� |
| B��n��B��=n��C�� |
| C��n��A��+n��B��=n��C�� |
| D��n��B��+n��C��=n��A�� |
ij�¶��£���Ӧ2CH3OH��g��?CH3OCH3��g��+H2O��g����ƽ�ⳣ��Ϊ400�����¶��£����ݻ�һ�����ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
����˵������ȷ���ǣ�������
| ���� | CH3OH | CH3OCH3 | H2O |
| Ũ��/��mol?L-1�� | 0.44 | 0.6 | 0.6 |
| A��CH3OH����ʼŨ��Ϊ1.64 mol/L |
| B����ʱ�淴Ӧ����С������Ӧ���� |
| C��ƽ��ʱ��CH3OH��Ũ��Ϊ0.04 mol/L |
| D��ƽ��ʱ��CH3OH��ת����С��90% |
N2��H2�����ʵ���֮��Ϊ2��3�Ļ���������һ�ݻ��̶����ܱ������У���һ���������·�����Ӧ�����ﵽƽ��ʱ�������ڵ�ѹǿΪ��Ӧ��ʼʱ��
����N2��ת����Ϊ��������
| 4 |
| 5 |
| A��50% | B��37.5% |
| C��25% | D��12.5% |
100mL 2mol/L�����������п��Ӧ��Ϊ�ӿ췴Ӧ���ʣ����ֲ�Ӱ�������������������ɲ�ȡ�Ĵ�ʩ�ǣ�������
| A�������¶� |
| B�����ú�����������ͭ��п |
| C������98%��Ũ���� |
| D����ˮ |
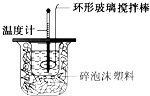 ijʵ��С����0.50mol?L-1 NaOH��Һ��0.55mol?L-1������Һ�����к��ȵIJⶨ��������0.50mol?L-1 NaOH��Һ
ijʵ��С����0.50mol?L-1 NaOH��Һ��0.55mol?L-1������Һ�����к��ȵIJⶨ��������0.50mol?L-1 NaOH��Һ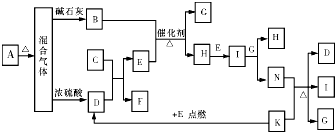 ��ͼ�е�B��K�ֱ�����йط�Ӧ��һ�ַ�Ӧ������������A��C��F��K�ǹ��壻E�dz��������嵥�ʣ�I�Ǻ���ɫ����̬�������̬����A���������Ⱥ����ɵ�����������ͨ����ʯ��ֻʣ������B����ͨ��Ũ������ֻʣ������D�������ʼ��ת����ϵ��ͼ��ʾ����ش��������⣺
��ͼ�е�B��K�ֱ�����йط�Ӧ��һ�ַ�Ӧ������������A��C��F��K�ǹ��壻E�dz��������嵥�ʣ�I�Ǻ���ɫ����̬�������̬����A���������Ⱥ����ɵ�����������ͨ����ʯ��ֻʣ������B����ͨ��Ũ������ֻʣ������D�������ʼ��ת����ϵ��ͼ��ʾ����ش��������⣺