题目内容
N2和H2的物质的量之比为2:3的混合气体充入一容积固定的密闭容器中,在一定的条件下发生反应,当达到平衡时,容器内的压强为反应开始时的
,则N2的转化率为( )
| 4 |
| 5 |
| A、50% | B、37.5% |
| C、25% | D、12.5% |
考点:化学平衡的计算
专题:化学平衡专题
分析:N2和H2的物质的量之比为2:3的混合气体充入一容积固定的密闭容器中,可以设其物质的量分别是2n和3n,当达到平衡时,容器内的压强为反应开始时的
,即当达到平衡时,容器内的物质的量为反应开始时的
,根据三行式计算即可.
| 4 |
| 5 |
| 4 |
| 5 |
解答:
解:设N2的转化量为x,则
N2+3H2 ?2NH3
初始量:2n 3n 0
变化量:x 3x 2x
平衡量:2n-x 3n-3x 2x
则
=
,解得x=0.5n,所以氮气的转化率=
×100%=25%,故选C.
N2+3H2 ?2NH3
初始量:2n 3n 0
变化量:x 3x 2x
平衡量:2n-x 3n-3x 2x
则
| 2n-x+3n-3x+2x |
| 5n |
| 4 |
| 5 |
| 0.5n |
| 2n |
点评:本题考查学生化学平衡的有关计算知识,注意化学反应前后物质的量之比等于压强之比这一结论,难度中等.

练习册系列答案
 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
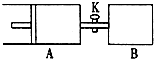 如图,容器A左侧是可平行移动的活塞.关闭活塞K,向A中充入1molX和1molY,向B中充入2molX和2molY,起始时A、B的体积都等于aL.在温度相同、外界压强相同和催化剂存在的条件下,使两容器各自发生反应:X(g)+Y(g)?Z(g)+2W(g).达平衡时,A的体积为1.2aL.下列说法正确的是( )
如图,容器A左侧是可平行移动的活塞.关闭活塞K,向A中充入1molX和1molY,向B中充入2molX和2molY,起始时A、B的体积都等于aL.在温度相同、外界压强相同和催化剂存在的条件下,使两容器各自发生反应:X(g)+Y(g)?Z(g)+2W(g).达平衡时,A的体积为1.2aL.下列说法正确的是( )| A、反应速率:V(B)<V(A) |
| B、A容器中X转化率为20% |
| C、平衡时的压强:P(B)=2P(A) |
| D、若打开K,则达到新的化学平衡时,A的体积为2.6aL |
向容积为2L的密闭容器中充入2mol A气体和1mol B气体,一定条件下发生如下反应2A(g)+B(g)?3C(g),经2s后达到平衡,测得C的浓度为0.6mol/L.下列说法中不正确的是( )
| A、用物质A表示该反应的平均反应速率为0.2mol?L-1?s-1 |
| B、平衡时物质A和B的转化率相等 |
| C、平衡时物质B的浓度为0.2mol/L |
| D、若将容积体积压缩为1L,B的平衡浓度变为原来的2倍 |
在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g)?xC(g)+D(s),向甲中通入6mol A和2mol B,向乙中通入1.5mol A、0.5mol B和3mol C和2mol D,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
| A、若平衡时,甲、乙两容器中A的物质的量不相等,则x=3 |
| B、平衡时,甲、乙两容器中A、B的物质的量之比不相等 |
| C、平衡时甲中A的体积分数为40% |
| D、若平衡时两容器中的压强不相等,则两容器中压强之比为8:5 |
“春蚕到死丝方尽”,这里“丝”的主要成分是( )
| A、维生素 | B、蛋白质 |
| C、纤维素 | D、油脂 |
下列各组原子中,彼此化学性质一定相似的是( )
| A、2p轨道上只有一个空轨道的X原子与3p轨道上只有一个空轨道的Y原子 |
| B、原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 |
| C、原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| D、最外层都只有一个电子的X、Y原子 |