题目内容
下列叙述或操作正确的是( )
| A、浓硫酸具有强氧化性,稀硫酸无氧化性 |
| B、浓硫酸滴到蓝矾上,蓝矾变成白色粉末,体现了浓硫酸的脱水性 |
| C、稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌 |
| D、浓硫酸与铜的反应中,浓硫酸仅表现强氧化性 |
考点:浓硫酸的性质
专题:
分析:A.稀硫酸具有弱氧化性;
B.浓硫酸具有强吸水性;
C.浓硫酸稀释时,要将浓硫酸倒入水中不断搅拌;
D.根据元素化合价变化确定浓硫酸的性质.
B.浓硫酸具有强吸水性;
C.浓硫酸稀释时,要将浓硫酸倒入水中不断搅拌;
D.根据元素化合价变化确定浓硫酸的性质.
解答:
解:A.稀硫酸具有弱氧化性,其氧化性是H元素体现的,故A错误;
B.浓硫酸滴到蓝矾上,蓝矾变成白色粉末,体现了浓硫酸的吸水性,故B错误;
C.浓硫酸稀释时,浓硫酸稀释放出大量的热,放出的热量使局部受热而溅出液体,所以将浓硫酸倒入水中要不断搅拌,故C正确;
D.该反应方程式为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,该反应中S元素部分化合价不变,部分S元素化合价由+6价变为+4价,所以浓硫酸体现氧化性和酸性,故D错误;
故选C.
B.浓硫酸滴到蓝矾上,蓝矾变成白色粉末,体现了浓硫酸的吸水性,故B错误;
C.浓硫酸稀释时,浓硫酸稀释放出大量的热,放出的热量使局部受热而溅出液体,所以将浓硫酸倒入水中要不断搅拌,故C正确;
D.该反应方程式为:Cu+2H2SO4(浓)
| ||
故选C.
点评:本题考查了浓硫酸的性质,根据元素化合价变化确定物质的性质,知道浓硫酸稀释方法,注意不能将水倒入浓硫酸中,为易错点,题目较简单.

练习册系列答案
相关题目
化学方程式可简明地体现元素及其化合物的性质.已知:
氧化还原反应:2FeCl3+2HI═2FeCl2+I2+2HCl;
2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O
2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI;
3I2+6KOH═5KI+KIO3+3H2O
复分解反应:2HSCN+K2CO3═2KSCN+CO2↑+H2O; KCN+CO2+H2O═HCN+KHCO3
热分解反应:4NaClO
3NaCl+NaClO4;NaClO4
NaCl+2O2↑
下列说法不正确是( )
氧化还原反应:2FeCl3+2HI═2FeCl2+I2+2HCl;
2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O
2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI;
3I2+6KOH═5KI+KIO3+3H2O
复分解反应:2HSCN+K2CO3═2KSCN+CO2↑+H2O; KCN+CO2+H2O═HCN+KHCO3
热分解反应:4NaClO
| ||
| ||
下列说法不正确是( )
| A、酸性(水溶液):HSCN>H2CO3>HCN |
| B、还原性(碱性溶液):Fe(OH)2>I2>KIO3 |
| C、热稳定性:NaCl>NaClO4>NaClO |
| D、氧化性(酸性溶液):FeCl3>Co(OH)3>I2 |
在下列溶液中,各组离子一定能够大量共存的是( )
| A、常温下水电离出的c(OH-)=10-13的溶液中:Na+、ClO-、F-、K+ |
| B、能使广泛pH试纸显蓝色的溶液:K+、Ba2+、Cl-、Br- |
| C、含有大量Al3+的溶液:Na+、Cl-、S2-、OH- |
| D、能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO42- |
下列说法正确的是( )


| A、①表示化学反应2NO2(g)+O3(g)═N2O5(g)+O2(g)△H>0 |
| B、②表示25℃时,用0.1 mol/LCH3COOH溶液滴定20 mL 0.1 mol/LNaOH溶液,溶液的pH随加入酸体积的变化 |
| C、③表示10 mL 0.01 mol/L KMnO4酸性溶液与过量的0.1 mol/LH2C2O4溶液混合时,n (Mn2+)随时间的变化 |
| D、④表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |
下列说法正确的是( )
| A、常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 |
| B、为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C、用0.200 0 mol?L-1 NaOH标准溶液滴定HCl与CH3 COOH的混合液(混合液中两种酸的浓度均约为0.1 mol?L-1,至中性时,溶液中的酸未被完全中和 |
| D、相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol?L-1盐酸、③0.1 mol?L-1氯化镁溶液、④0.1 mol?L-1硝酸银溶液中,Ag+浓度:①>④=②>③ |
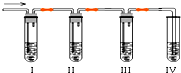 化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2.回答下列问题:
化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2.回答下列问题: