题目内容
化学方程式可简明地体现元素及其化合物的性质.已知:
氧化还原反应:2FeCl3+2HI═2FeCl2+I2+2HCl;
2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O
2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI;
3I2+6KOH═5KI+KIO3+3H2O
复分解反应:2HSCN+K2CO3═2KSCN+CO2↑+H2O; KCN+CO2+H2O═HCN+KHCO3
热分解反应:4NaClO
3NaCl+NaClO4;NaClO4
NaCl+2O2↑
下列说法不正确是( )
氧化还原反应:2FeCl3+2HI═2FeCl2+I2+2HCl;
2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O
2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI;
3I2+6KOH═5KI+KIO3+3H2O
复分解反应:2HSCN+K2CO3═2KSCN+CO2↑+H2O; KCN+CO2+H2O═HCN+KHCO3
热分解反应:4NaClO
| ||
| ||
下列说法不正确是( )
| A、酸性(水溶液):HSCN>H2CO3>HCN |
| B、还原性(碱性溶液):Fe(OH)2>I2>KIO3 |
| C、热稳定性:NaCl>NaClO4>NaClO |
| D、氧化性(酸性溶液):FeCl3>Co(OH)3>I2 |
考点:氧化性、还原性强弱的比较,钠的重要化合物
专题:
分析:A、根据化学反应遵循强酸制弱酸的规律来判断,在反应2HSCN+K2CO3═2KSCN+CO2↑+H2O中,酸性HSCN>H2CO3,在反应中 KCN+CO2+H2O═HCN+KHCO3,酸性H2CO3>HCN,则酸性为HSCN>H2CO3>HCN;
B、根据还原剂的还原性大于还原产物的还原性来判断,在3I2+6KOH═5KI+KIO3+3H2O反应中,还原性I2>KIO3;在2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI反应中,还原性Fe(OH)2>I2;
C、根据物质分解时生成更加稳定的物质来判断,在反应中4NaClO
3NaCl+NaClO4,稳定性NaClO4>NaClO,在反应中NaClO4
NaCl+2O2↑中,稳定性NaCl>NaClO4;
D、根据氧化剂的氧化性大于氧化产物的氧化性判断,在2FeCl3+2HI═2FeCl2+I2+2HCl反应中,氧化性:FeCl3>I2,在2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O中,氧化性:Co(OH)3>Cl2.
B、根据还原剂的还原性大于还原产物的还原性来判断,在3I2+6KOH═5KI+KIO3+3H2O反应中,还原性I2>KIO3;在2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI反应中,还原性Fe(OH)2>I2;
C、根据物质分解时生成更加稳定的物质来判断,在反应中4NaClO
| ||
| ||
D、根据氧化剂的氧化性大于氧化产物的氧化性判断,在2FeCl3+2HI═2FeCl2+I2+2HCl反应中,氧化性:FeCl3>I2,在2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O中,氧化性:Co(OH)3>Cl2.
解答:
解:A、化学反应遵循强酸制弱酸的规律,在反应2HSCN+K2CO3═2KSCN+CO2↑+H2O中,酸性HSCN>H2CO3,在反应中 KCN+CO2+H2O═HCN+KHCO3,酸性H2CO3>HCN,则酸性为HSCN>H2CO3>HCN,故A正确;
B、在3I2+6KOH═5KI+KIO3+3H2O反应中,I2既是氧化剂又是还原剂,其还原性介于高低价态产物之间KI>I2>KIO3;在2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI反应中,反应物中作还原剂的是该反应中所有物质中还原性最强的,即Fe(OH)2>I2;Fe(OH)2>Fe(OH)3;Fe(OH)2>KI,故还原性应为:Fe(OH)2>I2>KIO3,故B正确;
C、物质分解时生成更加稳定的物质,在反应中4NaClO
3NaCl+NaClO4,稳定性NaClO4>NaClO,在反应中NaClO4
NaCl+2O2↑中,稳定性NaCl>NaClO4,则稳定性NaCl>NaClO4>NaClO,故C正确;
D、在2FeCl3+2HI═2FeCl2+I2+2HCl反应中,氧化性:FeCl3>I2,在2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O中,氧化性:Co(OH)3>Cl2,又Cl2>FeCl3,故Co(OH)3>FeCl3,则有:Co(OH)3>FeCl3>I2,故D错误;
故选D.
B、在3I2+6KOH═5KI+KIO3+3H2O反应中,I2既是氧化剂又是还原剂,其还原性介于高低价态产物之间KI>I2>KIO3;在2Fe(OH)2+I2+2KOH═2Fe(OH)3+2KI反应中,反应物中作还原剂的是该反应中所有物质中还原性最强的,即Fe(OH)2>I2;Fe(OH)2>Fe(OH)3;Fe(OH)2>KI,故还原性应为:Fe(OH)2>I2>KIO3,故B正确;
C、物质分解时生成更加稳定的物质,在反应中4NaClO
| ||
| ||
D、在2FeCl3+2HI═2FeCl2+I2+2HCl反应中,氧化性:FeCl3>I2,在2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O中,氧化性:Co(OH)3>Cl2,又Cl2>FeCl3,故Co(OH)3>FeCl3,则有:Co(OH)3>FeCl3>I2,故D错误;
故选D.
点评:本题考查氧化性、还原性、稳定性和酸性的比较,做题时注意积累比较物质的性质的规律和方法.

练习册系列答案
相关题目
工业上用洗净的废铜屑作原料来制备硝酸铜.为了节约原料和防止污染环境,宜采用的方法是( )
| A、Cu+HNO3(浓)→Cu(NO3)2 |
| B、Cu+HNO3(稀)→Cu(NO3)2 |
| C、Cu+空气→CuO CuO+HNO3→Cu(NO3)2 |
| D、Cu+浓硫酸→CuSO4 CuSO4+Ba(NO3)2→Cu(NO3)2 |
苹果醋是一种由苹果发酵而形成的具有解毒、降脂、减肥等明显药效的健康食品.苹果酸(2羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构简式为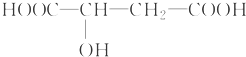 .下列相关说法不正确的是( )
.下列相关说法不正确的是( )
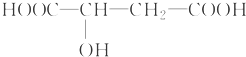 .下列相关说法不正确的是( )
.下列相关说法不正确的是( )| A、苹果酸在一定条件下能发生酯化反应 |
| B、苹果酸在一定条件下能发生催化氧化反应 |
| C、1 mol苹果酸与足量Na反应生成33.6 L H2(标准状况下) |
| D、1 mol苹果酸与Na2CO3溶液反应一定消耗2 mol Na2CO3 |
下列说法不正确的是( )
| A、常温下可以用铁、铝制容器盛放浓硫酸或浓硝酸 |
| B、氨气能使湿润的红色石蕊试纸变为蓝色 |
| C、“硅胶”常用作干燥剂,也可以做催化剂的载体 |
| D、NO和NO2均为无色的有毒的气体 |
下列叙述或操作正确的是( )
| A、浓硫酸具有强氧化性,稀硫酸无氧化性 |
| B、浓硫酸滴到蓝矾上,蓝矾变成白色粉末,体现了浓硫酸的脱水性 |
| C、稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌 |
| D、浓硫酸与铜的反应中,浓硫酸仅表现强氧化性 |
在蒸发皿中加热蒸干下列物质的溶液,再灼烧可以得到原溶质固体的是( )
| A、AlCl3 |
| B、NaHCO3 |
| C、MgSO4 |
| D、KMnO4 |
 验室用如图所示的装置制取乙酸乙酯.
验室用如图所示的装置制取乙酸乙酯. 在密闭容器中,一边装有一定量的金属钠,一边装有一定量的氧化汞,同时加热容器的两部分,钠和氧化汞都完全反应后,恢复到原温度,容器内空气的成分仍不变.则钠和氧化汞的物质的量之比是
在密闭容器中,一边装有一定量的金属钠,一边装有一定量的氧化汞,同时加热容器的两部分,钠和氧化汞都完全反应后,恢复到原温度,容器内空气的成分仍不变.则钠和氧化汞的物质的量之比是