题目内容
25℃时,0.01mol/L的稀盐酸溶液中水电离出的H+的浓度是( )
| A、5×10-13mol/L |
| B、0.01 mol/L |
| C、1×10-7 mol/L |
| D、1×10-12mol/L |
考点:水的电离
专题:
分析:0.01mol/L的盐酸中水电离的H+的浓度和水电离出氢氧离子浓度相等,抓住这一点来解题.
解答:
解:0.01mol/L的盐酸中氢氧根离子来自于水的电离,c(OH-)=
=
=10-12mol/L,而溶液中水电离的H+的浓度和水电离出氢氧离子浓度相等,
故选:D.
| KW |
| c(H+) |
| 10-14 |
| 0.01 |
故选:D.
点评:本题考查溶液PH的计算,和水的电离,学生只要认真分析,抓住水最离出的氢离子和氢氧根离子相等即可.

练习册系列答案
相关题目
下列关于电子云的说法中,正确的是( )
| A、电子云表示电子在原子核外运动的轨迹 |
| B、电子云表示电子在核外单位体积的空间出现的概率大小 |
| C、电子云界面图中的小黑点越密表示该核外空间的电子越多 |
| D、钠原子的1s、2s、3s电子云半径相同 |
如图是以石墨为电极,电解CuCl2溶液的装置图,下列说法正确的是( )
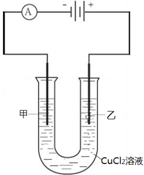

| A、甲电极为阳极 |
| B、阴极处能产生使湿润淀粉KI试纸变蓝的气体 |
| C、阴极发生还原反应 |
| D、通电时,溶液中的离子作定向运动 |
下列化合物中属于共价化合物的是( )
| A、NaCl |
| B、NaOH |
| C、CH4 |
| D、(NH4)2SO4 |
2.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)?PCl5(g) 达平衡时PCl5为0.40mol,如果此时再加入2.0mol PCl3和1.0mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
| A、小于0.40 mol |
| B、大于0.80 mol |
| C、等于0.80 mol |
| D、大于0.40 mol,小于0.80 mol |
一定条件下水分解生成氢气和氧气,有关物质和能量的转化关系如图所示,下列判断正确的是( )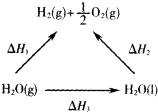

| A、△H1>△H2 |
| B、△H2<△H3 |
| C、△H1=△H2+△H3 |
| D、△H1+△H3>△H2 |
下列有关化学用语表示正确的是( )
A、H2S的电子式: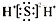 |
B、基态氧原子的电子排布图: |
| C、二氧化硅的分子式:SiO2 |
| D、24Cr的电子排布式:[Ar]3d54s1 |
 高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂.
高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂.