题目内容
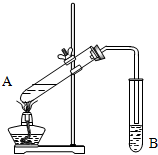 实验室用如图所示装置制取乙酸乙酯.
实验室用如图所示装置制取乙酸乙酯.(1)A试管中加药品的顺序为
(2)实验前向B试管中加入一滴酚酞试液,实验过程中观察到溶液的红色逐渐变浅,其原因是
(3)将生成的乙酸乙酯分离出来的实验操作是
(4)试管B中观察到的现象是
(5)请写出乙醇和乙酸发生酯化反应的化学方程式
(6)与乙醇和乙酸在浓硫酸催化作用下发生酯化反应相似,某酸和某醇也能发生酯化反应生成酯Cn+2H2n+4O2,若某酸表示为CnH2nO2,则某醇的结构简式为
考点:乙酸乙酯的制取
专题:有机物的化学性质及推断
分析:(1)浓硫酸密度大于乙醇,混合过程中放热大量热,则应该先加入乙醇,再加入浓硫酸,冷却后再加入乙酸;乙醇和乙酸的沸点较低,加热过程中容易发生暴沸,加入碎瓷片可以防止暴沸;B中液体是用于吸收生成的乙酸乙酯,通常使用的是饱和碳酸钠溶液,原因是乙酸乙酯在饱和碳酸钠溶液中的溶解度较小,碳酸钠能够中和乙酸、溶解乙醇;
(2)碳酸钠能够与挥发出来的乙酸发生反应,溶液碱性减弱;挥发出来的乙酸和乙醇易溶于饱和碳酸钠溶液,容易发生倒吸;
(3)乙酸乙酯不溶于饱和碳酸钠溶液,混合液体分层,可以通过分液操作分离出乙酸乙酯,分液操作的主要仪器是分液漏斗;乙酸乙酯的密度小于碳酸钠溶液,所以在混合液的上层;
(4)根据乙酸乙酯的密度、状态及味道等方面进行解答;
(5)乙酸与乙醇在浓硫酸作用下加热反应生成乙酸乙酯和水,据此写出反应的化学方程式;
(6)根据酯化反应原理“酸脱羟基醇脱氢”可知生成酯Cn+2H2n+4O2,是CnH2nO2和某醇脱去1分子水生成的,根据质量守恒定律可以计算出醇的分子式,然后确定结构简式.
(2)碳酸钠能够与挥发出来的乙酸发生反应,溶液碱性减弱;挥发出来的乙酸和乙醇易溶于饱和碳酸钠溶液,容易发生倒吸;
(3)乙酸乙酯不溶于饱和碳酸钠溶液,混合液体分层,可以通过分液操作分离出乙酸乙酯,分液操作的主要仪器是分液漏斗;乙酸乙酯的密度小于碳酸钠溶液,所以在混合液的上层;
(4)根据乙酸乙酯的密度、状态及味道等方面进行解答;
(5)乙酸与乙醇在浓硫酸作用下加热反应生成乙酸乙酯和水,据此写出反应的化学方程式;
(6)根据酯化反应原理“酸脱羟基醇脱氢”可知生成酯Cn+2H2n+4O2,是CnH2nO2和某醇脱去1分子水生成的,根据质量守恒定律可以计算出醇的分子式,然后确定结构简式.
解答:
解:(1)浓硫酸密度大于乙醇,所以应该先加乙醇,然后缓缓加入浓硫酸,同时用玻璃棒不断搅拌,冷却后加入乙酸;
给乙酸和乙醇的混合液体加热时容易发生暴沸现象,所以加入碎瓷片起到了防止暴沸的作用;
由于乙酸乙酯在饱和碳酸钠溶液中的溶解度较小,碳酸钠能够中和乙酸、溶解乙醇,便于混合液分层,
故答案为:先加乙醇,然后缓缓加入浓硫酸,同时用玻璃棒不断搅拌,冷却后加入乙酸;防止暴沸;饱和碳酸钠溶液;中和乙酸;吸收乙醇;降低乙酸乙酯的溶解度;
(2)碳酸钠溶液为碱性溶液,加入酚酞后溶液显示红色,实验过程中乙酸沸点降低,容易挥发出来,乙酸能够与碳酸钠溶液反应,碳酸钠浓度减小,溶液碱性减弱,溶液的红色逐渐变浅;乙醇和乙酸易溶于水,实验中注意长导管不能伸到B试管液面下,否则B试管中的液体倒吸进入A试管,发生倒吸现象,
故答案为:碳酸钠溶液与挥发出来的乙酸发生反应导致溶液的碱性逐惭减弱;防止倒吸;
(3)乙酸乙酯在饱和碳酸钠溶液中溶解度较小,反应后混合液分层,可以通过分液操作分离;分液操作使用的主要仪器为分液漏斗;乙酸乙酯在混合液上层,分液时应该从分液漏斗的上口倒出乙酸乙酯,
故答案为:分液;分液漏斗;上口倒;
(4)乙酸乙酯的密度小于碳酸钠溶液,且具有果香气味的油状液体,则试管B中观察到的现象为:在饱和碳酸钠溶液的液面上有一层无色、有果香味油状液体,
故答案为:在饱和碳酸钠溶液的液面上有一层无色、有果香味油状液体;
(5)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,反应的化学方程式为:CH3COOH+C2H5OH CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
故答案为:CH3COOH+C2H5OH CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(6)设醇的分子式为CxHyO,由于与乙醇和乙酸在浓硫酸催化作用下发生酯化反应相似,则CxHyO+CnH2nO2→Cn+2H2n+4O2+H2O,根据质量守恒,x=2、y=6,所以该醇的分子式为C2H6O,该醇为乙醇,结构简式为:CH3CH2OH,
故答案为:CH3CH2OH.
给乙酸和乙醇的混合液体加热时容易发生暴沸现象,所以加入碎瓷片起到了防止暴沸的作用;
由于乙酸乙酯在饱和碳酸钠溶液中的溶解度较小,碳酸钠能够中和乙酸、溶解乙醇,便于混合液分层,
故答案为:先加乙醇,然后缓缓加入浓硫酸,同时用玻璃棒不断搅拌,冷却后加入乙酸;防止暴沸;饱和碳酸钠溶液;中和乙酸;吸收乙醇;降低乙酸乙酯的溶解度;
(2)碳酸钠溶液为碱性溶液,加入酚酞后溶液显示红色,实验过程中乙酸沸点降低,容易挥发出来,乙酸能够与碳酸钠溶液反应,碳酸钠浓度减小,溶液碱性减弱,溶液的红色逐渐变浅;乙醇和乙酸易溶于水,实验中注意长导管不能伸到B试管液面下,否则B试管中的液体倒吸进入A试管,发生倒吸现象,
故答案为:碳酸钠溶液与挥发出来的乙酸发生反应导致溶液的碱性逐惭减弱;防止倒吸;
(3)乙酸乙酯在饱和碳酸钠溶液中溶解度较小,反应后混合液分层,可以通过分液操作分离;分液操作使用的主要仪器为分液漏斗;乙酸乙酯在混合液上层,分液时应该从分液漏斗的上口倒出乙酸乙酯,
故答案为:分液;分液漏斗;上口倒;
(4)乙酸乙酯的密度小于碳酸钠溶液,且具有果香气味的油状液体,则试管B中观察到的现象为:在饱和碳酸钠溶液的液面上有一层无色、有果香味油状液体,
故答案为:在饱和碳酸钠溶液的液面上有一层无色、有果香味油状液体;
(5)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,反应的化学方程式为:CH3COOH+C2H5OH
 CH3COOC2H5+H2O,
CH3COOC2H5+H2O,故答案为:CH3COOH+C2H5OH
 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;(6)设醇的分子式为CxHyO,由于与乙醇和乙酸在浓硫酸催化作用下发生酯化反应相似,则CxHyO+CnH2nO2→Cn+2H2n+4O2+H2O,根据质量守恒,x=2、y=6,所以该醇的分子式为C2H6O,该醇为乙醇,结构简式为:CH3CH2OH,
故答案为:CH3CH2OH.
点评:本题考查了乙酸乙酯的性质、制备方法、酯化反应原理,题目难度中等,试题题量较大,注意掌握乙酸乙酯的反应原理及实验室制法,明确酯化反应原理及饱和碳酸钠溶液、浓硫酸在试验中的作用.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
设NA为阿伏加德罗常数的值.下列关于0.2mol/L 硝酸钡溶液的不正确说法是( )
| A、1升溶液中所含阴、阳离子总数是0.6NA |
| B、1升溶液中含有0.2NA个NO3-离子 |
| C、500毫升溶液中的Ba2+离子浓度是0.2mol/L |
| D、500毫升溶液中的NO3-离子浓度是0.2mol/L |
下列说法中正确的是( )
| A、饮用水可以用明矾、漂白粉来净化,两者的作用原理相同 |
| B、常温常压下,78gNa2O2固体中所含阴离子数一定为NA |
| C、NH4Cl、MgCl2均为离子化合物,均含有离子键和共价键 |
| D、实验室中浓硝酸保存在带橡胶塞的棕色细口试剂瓶中 |
 铈、铬、钴、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.
铈、铬、钴、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用.
