��Ŀ����
2����⾫��ͭ���������к��д����Ĺ��ؽ����������ڵȷǽ���Ԫ�أ�ʵ���Ҵӵ�⾫��ͭ������������ȡ�����������������£�
��֪�����ʽ������Ի�������NaClO3��NaCl��Ӧ����NaAuCl4��NaAuCl4�ɱ�Fe2+��SO2��ԭΪ���ʽ����Ļ����ﲻ�ܱ�Fe2+��ԭ�����ܱ�SO2��ԭ��
��ش��������⣺
��1����������á���ͭҺ����ͭԪ�صĴ�����̬ΪCu2+���û�ѧʽ��ʾ��������ϡ�����Ŀ�����ṩ���Ի���������Fe3+��ˮ�⣮
��2��д��������н�Ԫ�ؽ��롰�Ȼ�Һ�������ӷ�Ӧ����ʽ2Au+ClO3-+7Cl-+6H+=2AuCl4-+3H2O����Ԫ�ؽ��롰�Ȼ������У�������ڵ���̬ΪAgCl���û�ѧʽ��ʾ����
��3������������Ȼ�Һ�м����ʵ����Լ�����ѡ����Լ�ΪA������ţ���
A��FeSO4•7H2O b��FeCl3 c��SO2 d��Na2SO3
�����Ȼ�Һ����c��AuCl4-��Ϊ0.01mol•L-1������500mL�á��Ȼ�Һ�������ĸ����ʵ�����Ϊ4.17g��
��4������ڿ���ͨ�����ķ����õ�����ͭ������ʱ�����ĵ缫��ӦʽΪCu2++2e-=Cu���ڲ�����У���Ԫ�ر������������ᣬ������ƴ����Ļ�ѧ��Ӧ����ʽH2SeO3+2SO2+H2O=Se��+H2SO4��
���� ��⾫��ͭ��������������ᡢ��������Cu���Է�Ӧ������ͭҺ���п�������ͭ�����������ȣ���ͭ���������ᡢ�����ơ��Ȼ��ƣ��Ȼ������Ի���Ag���Ȼ���ΪAgCl���Ȼ�Һ�к���NaAuCl4�����Ļ���������Ŀ��Ϣ��֪����Fe2+�õ����ʽ𣬶����Ļ����ﲻ��Fe2+��ԭ�����˷����Ļ�ԭҺװ������SO2��ԭ�õ�������
��1����������á���ͭҺ���к�������ͭ��������ˮ������ԣ�����������ˮ�⣻
��2�����ʽ������Ի�������NaClO3��NaCl��Ӧ����NaAuCl4����Ԫ���غ��֪������ˮ�����Ȼ�����Ϊ�Ȼ�����
��3��������ǽ�NaAuCl4��ԭΪ���ʽ𣬶����Ļ����ﲻ�ܱ���ԭ��Ӧѡ��FeSO4•7H2O��
����n=cV����n��AuCl4-�������ʵ��������ݵ���ת���غ����FeSO4•7H2O�����ʵ������ٸ���m=nM�������������
��4������ڿ���ͨ�����ķ����õ�����ͭ��������ͭ���ӷ�����ԭ��Ӧ�õ�Cu���ڲ�����У���Ԫ�ر������������ᣬ����������������������Ӧ�õ�Se��������������Ϊ���ᣮ
��� �⣺��⾫��ͭ��������������ᡢ��������Cu���Է�Ӧ������ͭҺ���п�������ͭ�����������ȣ���ͭ���������ᡢ�����ơ��Ȼ��ƣ��Ȼ������Ի���Ag���Ȼ���ΪAgCl���Ȼ�Һ�к���NaAuCl4�����Ļ���������Ŀ��Ϣ��֪����Fe2+�õ����ʽ𣬶����Ļ����ﲻ��Fe2+��ԭ�����˷����Ļ�ԭҺװ������SO2��ԭ�õ�������
��1����������á���ͭҺ���к�������ͭ��ͭԪ����Cu2+��ʽ������̬��������ˮ������ԣ����������ṩ���Ի���������Fe3+��ˮ�⣬
�ʴ�Ϊ��Cu2+���ṩ���Ի���������Fe3+��ˮ�⣻
��2�����ʽ������Ի�������NaClO3��NaCl��Ӧ����NaAuCl4����Ԫ���غ��֪������ˮ����Ӧ���ӷ���ʽΪ��2Au+ClO3-+7Cl-+6H+=2AuCl4-+3H2O����Ԫ�ؽ��롰�Ȼ������У�������ڵ���̬ΪAgCl��
�ʴ�Ϊ��2Au+ClO3-+7Cl-+6H+=2AuCl4-+3H2O��AgCl��
��3��������ǽ�NaAuCl4��ԭΪ���ʽ𣬶����Ļ����ﲻ�ܱ���ԭ��NaAuCl4�ɱ�Fe2+��ԭΪ���ʽ𣬣����Ļ����ﲻ�ܱ�Fe2+��ԭ��ѡ��FeSO4•7H2O����ԭ����
n��AuCl4-�������ʵ���=0.5L��0.01mol/L=0.005mol�����ݵ���ת���غ���ҪFeSO4•7H2O�����ʵ���Ϊ$\frac{0.005mol��3}{1}$=0.015mol������ҪFeSO4•7H2O ������Ϊ0.015mol��278g/mol=4.17g��
�ʴ�Ϊ��A��4.17��
��4������ڿ���ͨ�����ķ����õ�����ͭ��������ͭ���ӷ�����ԭ��Ӧ�õ�Cu�������缫��ӦʽΪ��Cu2++2e-=Cu���ڲ�����У���Ԫ�ر������������ᣬ����������������������Ӧ�õ�Se��������������Ϊ���ᣬ��Ӧ����ʽΪ��H2SeO3+2SO2+H2O=Se��+H2SO4��
�ʴ�Ϊ��Cu2++2e-=Cu��H2SeO3+2SO2+H2O=Se��+H2SO4��
���� �������ڻ�ѧ����������Ŀ���ؼ��ǹ������̵����⣬��������Ԫ�ػ��������ʣ����ؿ���ѧ����ȡ��Ϣ��Ǩ������������������ԭ��Ӧ���㡢���ʵķ����ᴿ�ȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | �ϳɰ��Ļ�ѧ��Ӧ����� | |
| B�� | N2��ת������� | |
| C�� | �����Ļ������ | |
| D�� | NH3��ƽ���������е����������� |
| A�� | MnO2��Ũ���ᷴӦ��Cl2��MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2Cl-+Cl2��+2H2O | |
| B�� | �Ȼ�����Һ�μӵ���ˮ�еõ�Fe��OH��3 ���壺Fe3++3H2O�TFe��OH��3��+3H+ | |
| C�� | �������������H2��2Fe+6H+�T2Fe3++3H2�� | |
| D�� | Ca��HCO3��2��Һ������NaOH��Һ��Ӧ��HCO3-+Ca2++OH-�TCaCO3��+H2O |
| A�� | ��Ȼ����û���κ�һ��ʳ����ͬʱ��������Ը���ά���ص���Ҫ | |
| B�� | ����2008�걱�����ˡ����ơ����ı�����һ�����ȼ�� | |
| C�� | �ô�����ľ���һ���������ܷⱣ�棬ʱ��Խ��Խ�㴼 | |
| D�� | �����ǡ����ǡ���ά�غ�֬����һ�������¶����Է���ˮ�ⷴӦ |
| A�� | NaNO2�ǻ�ԭ�� | |
| B�� | NH4Cl��NԪ�ر���ԭ | |
| C�� | ����1 mol N2ʱת��6 mol���� | |
| D�� | �������ͻ�ԭ�������ʵ���֮����1��1 |
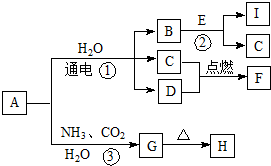 ��ѧ��ѧ�е�һЩ������������ͼת����ϵ�����ֲ���δ������������A����ɫ�ʻ�ɫ��D������Ϊ����ɫ���壬��Ӧ��Ϊ�����Ƽ��Ӧԭ��֮һ��E�dz����Ľ�����
��ѧ��ѧ�е�һЩ������������ͼת����ϵ�����ֲ���δ������������A����ɫ�ʻ�ɫ��D������Ϊ����ɫ���壬��Ӧ��Ϊ�����Ƽ��Ӧԭ��֮һ��E�dz����Ľ�����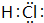 ��
��