题目内容
12.下列离子方程式书写正确的是( )| A. | 氧化钠与水反应:O2-+2H2O═2OH- | |
| B. | 氯气通入溴化钠溶液中:Cl2+2Br-═2Cl-+Br2 | |
| C. | 硫酸铜溶液与氢氧化钡溶液混合:SO42-+Ba2+═BaSO4↓ | |
| D. | 氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2Cl- |
分析 A.氧化物要写化学式;
B.二者发生置换反应生成氯化钠和溴;
C.漏写生成氢氧化铜沉淀的离子方程式;
D.转移电子不守恒、电荷不守恒.
解答 解:A.氧化物要写化学式,离子方程式为Na2O+H2O=2Na++2OH-,故A错误;
B.二者发生置换反应生成氯化钠和溴,离子方程式为Cl2+2Br-═2Cl-+Br2,故B正确;
C.漏写生成氢氧化铜沉淀的离子方程式,离子方程式为Cu2++2OH-+Ba2++SO42-=BaSO4↓+Cu(OH)2↓,故C错误;
D.转移电子不守恒、电荷不守恒,离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,故D错误;
故选B.
点评 本题考查离子方程式正误判断,为高频考点,明确离子方程式书写规则及离子性质是解本题关键,注意要遵循原子守恒、电荷守恒、转移电子守恒,易错选项是C.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
2.醇类物质中,具有“-CH2OH”结构的才能被氧化成相应的酸.分子式为C5Hl2O可被氧化成酸的醇共有( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
3.能正确表示下列反应的离子方程式是( )
| A. | Fe3O4与稀硝酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| B. | NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 向FeCl3溶液中加入少量KSCN溶液:Fe3++3SCN-═Fe(SCN)3↓ |
20.下列说法正确的是( )
| A. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| B. | 淀粉和蛋白质水解的最终产物都能发生银镜反应 | |
| C. | 油脂都是高级脂肪酸甘油酯,在碱性条件下能发生皂化反应 | |
| D. | “乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物 |
7.35Cl和35Cl-两种微粒中,不同的是( )
| A. | 核内质子数 | B. | 核外电子层数 | C. | 核内中子数 | D. | 核外电子数 |
17.下列各组离子,在强酸性溶液中能大量共存的是( )
| A. | Na+、K+、Ca2+、HCO3- | B. | NO3-、Cl-、Na+、Ag+ | ||
| C. | Cu2+、Fe2+、SO42-、Cl- | D. | Mg2+、Na+、Cl-、CH3COO- |
1.下列物质发生反应时,不因为反应的条件、反应物浓度或反应物的用量不同,而产物不同的是( )
| A. | 钠与氧气 | B. | 碳与氧气 | C. | 硅和氯气 | D. | 铁和硫酸 |
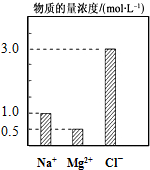 在200mL由NaCl、MgCl2、KCl组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在200mL由NaCl、MgCl2、KCl组成的混合液中,部分离子浓度大小如图所示,回答下列问题: