题目内容
16.在酸性溶液中,下列离子不能大量存在的是( )| A. | Mg2+ | B. | OHˉ | C. | SO42- | D. | Fe3+ |
分析 酸性溶液中含有大量氢离子,能和氢离子反应的离子不能大量共存,据此分析解答.
解答 解:A.镁离子和氢离子不反应,所以能大量共存,故A不选;
B.氢离子和氢氧根离子反应生成弱电解质水,所以不能大量共存,故B选;
D.氢离子和硫酸根离子不反应,所以能大量共存,故C不选;
D.铁离子和氢离子不反应,所以能大量共存,故D不选;
故选B.
点评 本题考查离子共存,为高频考点,明确离子性质及离子共存体积是解本题关键,生成弱电解质、气体、沉淀或发生氧化还原反应、双水解反应、络合反应的离子不能大量共存,题目难度不大.

练习册系列答案
相关题目
6.下列解释过程或事实的方程式不正确的是( )
| A. | Na放入水中,产生气体:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 用催化法处理汽车尾气中的CO和NO:CO+NO$\frac{\underline{\;催化剂\;}}{\;}$C+NO2 | |
| C. | NaOH溶液不能保存在玻璃塞的试剂瓶中:SiO2+2OH-═SiO32-+H2O | |
| D. | 红热的铁丝与水蒸汽接触,表面形成蓝黑色(或黑色)保护层:3Fe+4H2O(气)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2 |
7.35Cl和35Cl-两种微粒中,不同的是( )
| A. | 核内质子数 | B. | 核外电子层数 | C. | 核内中子数 | D. | 核外电子数 |
11.与KCl的化学键类型相同的物质是( )
| A. | H2O | B. | HCl | C. | MgCl2 | D. | SO2 |
1.下列物质发生反应时,不因为反应的条件、反应物浓度或反应物的用量不同,而产物不同的是( )
| A. | 钠与氧气 | B. | 碳与氧气 | C. | 硅和氯气 | D. | 铁和硫酸 |
5.某烃的分子式为C4H8,已知它能使酸性KMnO4溶液褪色,完全燃烧时生成等物质的量的CO2与H2O,则它与HBr加成反应时,最多可得到几种不同(不考虑立体异构)的产物( )
| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
4.关于0.2mol/L的NaOH溶液,下列说法错误的是( )
| A. | 100mL该溶液中含0.8g NaOH | |
| B. | 200mL该溶液与100mL 0.2 mol/L的硫酸溶液反应形成中性溶液 | |
| C. | 100mL该溶液中约含0.02 mol×6.02×1023mol-1个Na+ | |
| D. | 取NaOH 8g溶于1L水中即得到1L该溶液 |
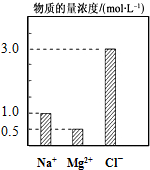 在200mL由NaCl、MgCl2、KCl组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在200mL由NaCl、MgCl2、KCl组成的混合液中,部分离子浓度大小如图所示,回答下列问题: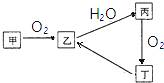 已知甲、乙、丙、丁4种物质均含有常见非金属元素,其中甲为淡黄色粉末.它们之间有如图所示的转化关系(转化过程中部分产物未标出).
已知甲、乙、丙、丁4种物质均含有常见非金属元素,其中甲为淡黄色粉末.它们之间有如图所示的转化关系(转化过程中部分产物未标出).