题目内容
下列说法正确的是( )
| A、食用加碘盐可预防碘缺乏症,加碘盐中加的含碘物质是碘单质 |
| B、因为NaCl的水溶液能导电,所以NaCl溶液属于强电解质 |
| C、电解熔融NaCl得到23.0g金属钠时能产生22.4 L氯气(标准状况下) |
| D、37Cl 是氯元素的一种同位素,23Na37Cl中质子数和中子数之比是7:8 |
考点:氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:A、食用加碘盐可预防碘缺乏症,加碘盐中加的含碘物质是碘酸钾;
B、电解质是化合物,NaCl溶液是混合物;
C、利用电解反应中氯化钠的物质的量来计算电解产物的量即可解答;
D、23Na37Cl中质子数和中子数分别是28和32.
B、电解质是化合物,NaCl溶液是混合物;
C、利用电解反应中氯化钠的物质的量来计算电解产物的量即可解答;
D、23Na37Cl中质子数和中子数分别是28和32.
解答:
解:A、食用加碘盐可预防碘缺乏症,加碘盐中加的含碘物质是碘酸钾,故A错误;
B、电解质是化合物,NaCl溶液是混合物,不属于电解质,故B错误;
C、得到23g金属钠,则需要电解58.5g熔融的NaCl,能产生0.5mol×22.4L/mol=11.2L氯气(标准状况),而不是22.4L氯气,故C错误;
D、23Na37Cl中质子数和中子数分别是28和32,所以质子数和中子数之比是7:8,故D正确.
故选:D.
B、电解质是化合物,NaCl溶液是混合物,不属于电解质,故B错误;
C、得到23g金属钠,则需要电解58.5g熔融的NaCl,能产生0.5mol×22.4L/mol=11.2L氯气(标准状况),而不是22.4L氯气,故C错误;
D、23Na37Cl中质子数和中子数分别是28和32,所以质子数和中子数之比是7:8,故D正确.
故选:D.
点评:本题考查微观粒子的物质的量的计算,明确物质的构成、电解等知识点来解答,学生熟悉物质的量的计算、利用原子守恒来判断电解产物的物质的量是解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
酒后驾车是引发交通事故的重要原因.交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿包Cr3+.下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低②乙醇密度比水小③乙醇有还原性④乙醇是烃的含氧衍生物⑤乙醇有刺檄性气味.
①乙醇沸点低②乙醇密度比水小③乙醇有还原性④乙醇是烃的含氧衍生物⑤乙醇有刺檄性气味.
| A、②④⑤ | B、②③ | C、①③ | D、①④ |
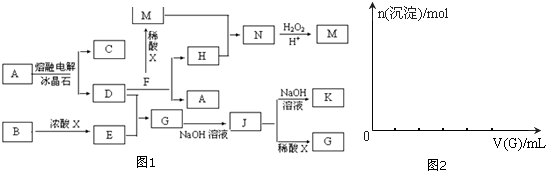
下图所示为海水综合利用部分流程,有关说法错误的是:( )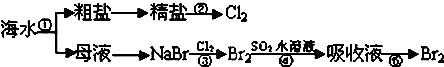
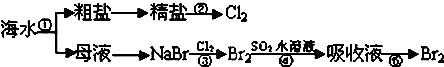
| A、实验室进行①的操作需用到坩埚、玻璃棒、酒精灯 |
| B、②是一个将电能转化为化学能的过程 |
| C、③④⑤涉及的反应均为氧化还原反应 |
| D、NaCl溶液蒸发结晶时,蒸发皿中有大量晶体析出时停止加热 |
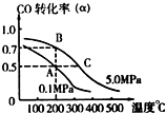 密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)=CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示.下列说法正确的是( )
密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)=CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示.下列说法正确的是( )| A、在 A、B两点对应的容器中,n(A)总:n(B)总=4:5 |
| B、在 A、C两点对应的容器中自反应开始到平衡状态所需的时间tA,<tC |
| C、设B、C两点的平衡常数分别为KB、KC,则KB<KC |
| D、在不改变反应物用量的情况下,降温、加压、将甲醇从混合体系中分离出来均可提高CO的转化率 |
设NA表示阿伏加德罗常数的值.下列叙述不正确的是( )
| A、1molNa2O和Na2O2的混合物中含有的阴、阳离子总数是3NA |
| B、常温下,1L0.1 mol?L-1的NH4NO3溶液中含有的氮原子数为0.2NA |
| C、46g有机物C2H6O中含有的H-O键的数目为NA |
| D、标准状况下,将0.1molCl2通入足量NaOH溶液中,反应转移的电子数为0.1NA |
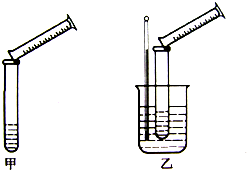 硫代硫酸钠与稀硫酸的反应为:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O.某实验兴趣小组用如下图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)
硫代硫酸钠与稀硫酸的反应为:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O.某实验兴趣小组用如下图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略) 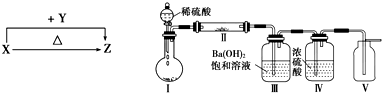
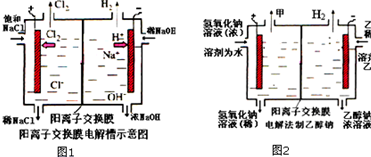 工业上生产氯气,常用电解槽电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分.如图1为电解槽的示意图.
工业上生产氯气,常用电解槽电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分.如图1为电解槽的示意图.