题目内容
15.如图是在明矾溶液中滴入氢氧化钡溶液,下列说法错误的是( )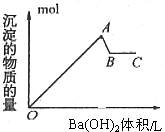
| A. | OA段的反应离子方程式为:2Al3++3SO42-+3Ba2++6OH-→2Al(OH)3↓+3BaSO4↓ | |
| B. | AB段的离子方程式只有:Al(OH)3+OH-→AlO2-+2H2O | |
| C. | A点的沉淀为Al(OH)3和BaSO4的混合物 | |
| D. | B点溶液为KAlO2溶液 |
分析 向明矾溶液里滴加氢氧化钡溶液,开始到生成沉淀的物质的量最大时:2Al3++3SO42-+3Ba2++6OH-→2Al(OH)3↓+3BaSO4↓;继续加氢氧化钡,当硫酸根离子恰好沉淀完全时,发生KAl(SO4)2+2Ba(OH)2═2BaSO4↓+KAlO2+2H2O,以此来解答.
解答 解:向明矾溶液里滴加氢氧化钡溶液,开始到生成沉淀的物质的量最大时:2Al3++3SO42-+3Ba2++6OH-→2Al(OH)3↓+3BaSO4↓;继续加氢氧化钡,当硫酸根离子恰好沉淀完全时,发生KAl(SO4)2+2Ba(OH)2═2BaSO4↓+KAlO2+2H2O,
A.OA段生成沉淀的物质的量最大,反应离子方程式为:2Al3++3SO42-+3Ba2++6OH-→2Al(OH)3↓+3BaSO4↓,故A正确;
B.AB段氢氧化铝溶解,钡离子与硫酸根离子生成沉淀,则离子方程式为2SO42-+2Ba2++Al(OH)3+OH-=AlO2-+2BaSO4↓+2H2O,故B错误;
C.OA段生成沉淀的物质的量最大,沉淀为Al(OH)3和BaSO4的混合物,故C正确;
D.AB段氢氧化铝溶解,SO42-全部转化为BaSO4,则B点溶液为KAlO2,故D正确.
故选B.
点评 本题考查离子反应、离子方程式的书写等,明确硫酸根离子完全沉淀时消耗的氢氧化钡的量是解答本题的关键,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
6.针对下面10种元素,完成以下各小题.回答下列间题.
(1)非金属性最强的元素是氟(填名称).化学性质最不活泼的元素是Ne(填元素符号).
(2)S 原子结构示意图为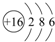 ;
;
(3)Mg和Al中,原子半径较小的是Al;
(4)N的氢化物的分子式NH3,该物质中N元素与H元素的质量比为14:3,(相对原子质量:N-14 H-1),其水溶液呈碱性性.
(5)元素硅的氧化物常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(6)元素最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式),呈两性的是Al(OH)3(填化学式);两者反应的化学方程式NaOH+Al(OH)3=NaAlO2+2H2O.
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | C | N | F | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)S 原子结构示意图为
 ;
;(3)Mg和Al中,原子半径较小的是Al;
(4)N的氢化物的分子式NH3,该物质中N元素与H元素的质量比为14:3,(相对原子质量:N-14 H-1),其水溶液呈碱性性.
(5)元素硅的氧化物常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(6)元素最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式),呈两性的是Al(OH)3(填化学式);两者反应的化学方程式NaOH+Al(OH)3=NaAlO2+2H2O.
3.在标准状况下进行甲、乙、丙三组实验,三组实验均各取30mL同浓度的盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据如表:
(1)乙组实验中,盐酸过量(填“过量”、“适量”、“不足量”).
(2)要计算出盐酸的物质的量浓度,题中可作为计算依据的数据是乙或丙,求得盐酸的物质的量浓度为1mol/L.
(3)求合金中镁、铝的物质的量之比,题中可作为计算依据的数据是甲,求得的镁、铝的物质的量之比是1:1.
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(2)要计算出盐酸的物质的量浓度,题中可作为计算依据的数据是乙或丙,求得盐酸的物质的量浓度为1mol/L.
(3)求合金中镁、铝的物质的量之比,题中可作为计算依据的数据是甲,求得的镁、铝的物质的量之比是1:1.
10.PbO2在酸性溶液中能将Mn2+氧化成MnO4-,本身被还原为Pb2+.取一支试管,加入适量PbO2固体和适量的稀H2SO4后滴入2mL 1mol/L MnSO4溶液.下列说法错误的是( )
| A. | 上述实验中不能用盐酸代替硫酸 | |
| B. | 将试管充分振荡后静置,溶液颜色变为紫色 | |
| C. | 在酸性条件下,PbO2的氧化性比MnO4-的氧化性强 | |
| D. | 若硫酸锰充分反应,消耗PbO2的物质的量为0.01mol |
7.R分子的质量为a g,相对质量为M,则M与a的比值等于( )
| A. | 6.02×1023 | B. | 12C原子质量的十二分之一 | ||
| C. | 0.012Kg12C所含的原子数 | D. | 1mol氧气所含的微粒数 |
4.青蒿素结构如图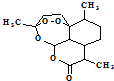 ,有关叙述正确的是d(选填序号).
,有关叙述正确的是d(选填序号).
a.化学式为C15H21O5 b.不能与NaOH溶液反应
c.易溶于水 d.含有过氧键,有较强氧化性
由青蒿酸为原料出发,经五步合成可得到青蒿素.其中第2步为还原反应: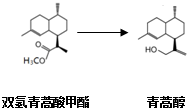
常温下即可反应且略放热,还原剂为LiAlH4.相关物质的性质:
某学习小组在实验室用双氢青蒿酸甲酯制取青蒿醇.
(1)反应中使用过量的氢化铝锂,理由是提高双氢青蒿酸甲酯的转化率.
为使反应在溶液状态下进行,可用乙醚为溶剂,不用水的理由是双氢青蒿酸甲酯不溶于水,氢化铝锂会与水反应.
(2)请设计实验室制备装置(画出草图):

(3)该反应有机物的转化率约为96%,所得乙醚溶液中含有醇锂、醇铝、双氢青蒿酸甲酯、氢化铝锂.从反应混合物中提取青蒿醇的方法是:
①加盐酸后分液;
②从乙醚层提取青蒿醇.有多种方法,以下是二种方案:
方案一:蒸发结晶. 方案二:蒸馏析出晶体.
a.这2个方案在析出晶体后都应有残留液,原因是防止氢青蒿酸甲酯析出.
b.请对这2个方案进行比较方案二可回收乙醚、甲醇.
 ,有关叙述正确的是d(选填序号).
,有关叙述正确的是d(选填序号).a.化学式为C15H21O5 b.不能与NaOH溶液反应
c.易溶于水 d.含有过氧键,有较强氧化性
由青蒿酸为原料出发,经五步合成可得到青蒿素.其中第2步为还原反应:

常温下即可反应且略放热,还原剂为LiAlH4.相关物质的性质:
| 物质 | 性质 |
| 双氢青蒿酸甲酯(C16H28O2) | 固体,难溶于水,易溶于有机溶剂. |
| 青蒿醇(C15H28O) | 固体,难溶于水,易溶于有机溶剂. |
| 乙醚 | 无色液体,微溶于水;密度0.71g/cm3;沸点:34.6℃. |
| 氢化铝锂 | 固体,溶于乙醚. 与水反应:LiAlH4+4H2O→Al(OH)3↓+LiOH+4H2↑ 可将一分子酯还原成二分子醇,自身生成醇铝、醇锂. (醇铝、醇锂可与盐酸反应,生成铝盐、锂盐和相应的醇). |
(1)反应中使用过量的氢化铝锂,理由是提高双氢青蒿酸甲酯的转化率.
为使反应在溶液状态下进行,可用乙醚为溶剂,不用水的理由是双氢青蒿酸甲酯不溶于水,氢化铝锂会与水反应.
(2)请设计实验室制备装置(画出草图):

(3)该反应有机物的转化率约为96%,所得乙醚溶液中含有醇锂、醇铝、双氢青蒿酸甲酯、氢化铝锂.从反应混合物中提取青蒿醇的方法是:
①加盐酸后分液;
②从乙醚层提取青蒿醇.有多种方法,以下是二种方案:
方案一:蒸发结晶. 方案二:蒸馏析出晶体.
a.这2个方案在析出晶体后都应有残留液,原因是防止氢青蒿酸甲酯析出.
b.请对这2个方案进行比较方案二可回收乙醚、甲醇.
5.关于晶体的说法正确的是( )
| A. | 若晶体熔融状态下能导电,该晶体一定是离子晶体 | |
| B. | 若晶体熔化时化学键断裂,该晶体一定是原子晶体 | |
| C. | 若晶体中含有非极性分子,该晶体可能有较低的熔沸点 | |
| D. | 若晶体中含有极性共价键,该晶体不可能有很高的熔沸点 |
 .
.