题目内容
7.R分子的质量为a g,相对质量为M,则M与a的比值等于( )| A. | 6.02×1023 | B. | 12C原子质量的十二分之一 | ||
| C. | 0.012Kg12C所含的原子数 | D. | 1mol氧气所含的微粒数 |
分析 R分子的相对质量为M,故可知R的摩尔质量为Mg/mol,即1molR的质量为Mg,由于一个R分子的质量为ag,故可知$\frac{M}{a}$的意义是在1molR中即MgR中含有的R分子的个数,据此分析.
解答 解:R分子的相对质量为M,故R的摩尔质量为Mg/mol,即1molR的质量为Mg,而一个R分子的质量为ag,故$\frac{M}{a}$的意义是在MgR中即1molR中所含有的R分子的个数,即6.02×1023个,即0.012Kg12C所含的原子数,故AC正确.
故选AC.
点评 本题考查了阿伏伽德罗常数的计算和含义,应注意的是1mol物质中含有NA个微粒,即NA个微粒的质量之和即1mol物质的质量.难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.在有机化工中,氯气是合成塑料、橡胶、农药和染料等的重要原料.下列关于氯气性质的描述不正确的是( )
| A. | 无气味 | B. | 能溶于水 | C. | 能与水反应 | D. | 能与铜反应 |
18.下列叙述正确的是( )
(1)二氧化硫使品红溶液,溴水和酸性高锰酸钾溶液褪色是因为二氧化硫具有漂白性.
(2)二氧化硫溶于水得到的溶液有氧化性,还原性,酸性.
(3)二氧化硫通入氢氧化钡溶液中,有白色沉淀生成,加入盐酸沉淀溶解.
(4)二氧化硫通入氯化钡溶液中有沉淀生成.
(1)二氧化硫使品红溶液,溴水和酸性高锰酸钾溶液褪色是因为二氧化硫具有漂白性.
(2)二氧化硫溶于水得到的溶液有氧化性,还原性,酸性.
(3)二氧化硫通入氢氧化钡溶液中,有白色沉淀生成,加入盐酸沉淀溶解.
(4)二氧化硫通入氯化钡溶液中有沉淀生成.
| A. | (1)(4) | B. | (4)(3) | C. | (1)(2) | D. | (2)(3) |
15.如图是在明矾溶液中滴入氢氧化钡溶液,下列说法错误的是( )
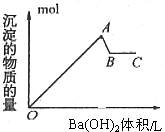

| A. | OA段的反应离子方程式为:2Al3++3SO42-+3Ba2++6OH-→2Al(OH)3↓+3BaSO4↓ | |
| B. | AB段的离子方程式只有:Al(OH)3+OH-→AlO2-+2H2O | |
| C. | A点的沉淀为Al(OH)3和BaSO4的混合物 | |
| D. | B点溶液为KAlO2溶液 |
2.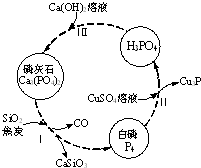 磷及部分重要化合物的相互转化如图所示.
磷及部分重要化合物的相互转化如图所示.
(1)不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为0.05mol.
(2)步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有Ca (H2PO4)2、CaHPO4.
磷灰石是生产磷肥的原料,它的组成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析结果如下(各元素均以氧化物形式表示):
(3)磷灰石中,碳元素的质量分数为1.66%%(保留两位小数).
(4)取100g磷灰石粉末,加入足量的浓硫酸,并加热,钙元素全部以CaSO4的形式存在,可以得到CaSO4114.87g(保留两位小数).
(5)取m g 磷灰石粉末,用50.00mL混酸溶液(磷酸为0.5mol/L、硫酸为0.1mol/L)与其反应,结果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值.
 磷及部分重要化合物的相互转化如图所示.
磷及部分重要化合物的相互转化如图所示.(1)不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为0.05mol.
(2)步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有Ca (H2PO4)2、CaHPO4.
磷灰石是生产磷肥的原料,它的组成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析结果如下(各元素均以氧化物形式表示):
| 成分 | CaO | P2O5 | SO3 | CO2 |
| 质量分数(%) | 47.30 | 28.40 | 3.50 | 6.10 |
(4)取100g磷灰石粉末,加入足量的浓硫酸,并加热,钙元素全部以CaSO4的形式存在,可以得到CaSO4114.87g(保留两位小数).
(5)取m g 磷灰石粉末,用50.00mL混酸溶液(磷酸为0.5mol/L、硫酸为0.1mol/L)与其反应,结果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值.
12.关于35℃的0.1mol/L NaOH溶液,以下表述错误的是( )
| A. | Kw>1×10-14 | B. | 水电离的c(H+)>1×10-13 mol/L | ||
| C. | pH>13 | D. | c(OH-)=c(H+)+c(Na+) |
19.NaHS溶液中加入一定量的CuSO4溶液,发生的反应的离子方程式可能为( )
| A. | S2-+Cu2+→CuS↓ | B. | 2HS-+Cu2+→CuS↓+2H++S2- | ||
| C. | HS-+Cu2+→CuS↓+H+ | D. | 2HS-+Cu2+→CuS↓+H2S↑ |
16.某温度下,浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,该溶液呈中性的依据是( )
| A. | a=b | B. | HA与BOH的电离常数相等 | ||
| C. | 混合溶液中,c(H+)=$\sqrt{{K}_{W}}$mol/L | D. | 混合溶液中,c(H+)+c(B+)═c(OH-)+c(A-) |