��Ŀ����
 ��1����6mol A�����5mol B�����Ϸ���4L�ܱ������У���һ�������·�����Ӧ��3A��g��+B��g��?2C��g��+xD��g������5min�ﵽƽ�⣬��ʱ����2mol C�����D��ƽ����Ӧ����Ϊ0.15mol/��L?min������
��1����6mol A�����5mol B�����Ϸ���4L�ܱ������У���һ�������·�����Ӧ��3A��g��+B��g��?2C��g��+xD��g������5min�ﵽƽ�⣬��ʱ����2mol C�����D��ƽ����Ӧ����Ϊ0.15mol/��L?min��������ƽ��ʱA�����ʵ���Ũ����
��������հ״�������ʽд������x�Ĺ��̣�
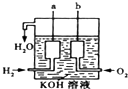
��2����������������ɴ���ʹ����һ������װ�ã��乹����ͼ��ʾ��a��b�����缫���ɶ��̼����ɣ�д��a���ĵ缫��Ӧʽ��
���㣺��ѧƽ��ļ���,ԭ��غ͵��صĹ���ԭ��
ר�⣺��ѧƽ��ר��,�绯ѧר��
��������1����c��A��ƽ��=
������ƽ��ʱC�����ʵ������������ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ������n��A����������n��A��ƽ��=n��A����ʼ-��n��A�������n��A��ƽ����������㣻���ݷ�Ӧ����=
���㣻
�ڸ���D�ķ�Ӧ�������D�����ʵ��������ݷ�Ӧ�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȼ���x��
��2������ȼ�ϵ���У�ͨ��������һ��Ϊ��Դ�ĸ���������������Ӧ���缫��ӦʽΪH2-2e-+2OH-=2H2O��ͨ��������һ��Ϊԭ��ص��������缫��ӦʽΪO2+4e-+2H2O=4OH-��ԭ��ع���ʱ������ȼ�ϵ�ص��ܷ�ӦΪ2H2+O2=2H2O��
| n |
| V |
| ��c |
| ��t |
�ڸ���D�ķ�Ӧ�������D�����ʵ��������ݷ�Ӧ�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȼ���x��
��2������ȼ�ϵ���У�ͨ��������һ��Ϊ��Դ�ĸ���������������Ӧ���缫��ӦʽΪH2-2e-+2OH-=2H2O��ͨ��������һ��Ϊԭ��ص��������缫��ӦʽΪO2+4e-+2H2O=4OH-��ԭ��ع���ʱ������ȼ�ϵ�ص��ܷ�ӦΪ2H2+O2=2H2O��
���
�⣺��1���١�n��A��=
��2mol=3mol����n��B��=
��2mol=1mol
n��A��ƽ��=n��A����ʼ-��n��A��=6mol-3mol=3mol��
����c��A��ƽ��=
=
=0.75mol/L��B��ת����=
��100%=20%
�ʴ�Ϊ��0.75mol/L��20%��
��D�����ʵ���Ϊn��D��=0.15mol?��L?min��-1��5min��4L=3mol����Ӧ�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ�����2��x=2mol��3mol�����x=3��
��x��ֵ��3��
��2������ȼ�ϵ���У�ͨ��������һ��Ϊ��Դ�ĸ�����ͨ��������һ��Ϊԭ��ص����������ڵ������Һ�ʼ��ԣ���a�缫��ӦʽΪ2H2-4e-+4OH-=4H2O����H2-2e-+2OH-=2H2O��������b�缫��ӦʽΪO2+4e-+2H2O=4OH-��
�ʴ�Ϊ��2H2-4e-+4OH-=4H2O����H2-2e-+2OH-=2H2O����
| 3 |
| 2 |
| 1 |
| 2 |
n��A��ƽ��=n��A����ʼ-��n��A��=6mol-3mol=3mol��
����c��A��ƽ��=
| n(A)ƽ�� |
| V |
| 3mol |
| 4L |
| 1mol |
| 5mol |
�ʴ�Ϊ��0.75mol/L��20%��
��D�����ʵ���Ϊn��D��=0.15mol?��L?min��-1��5min��4L=3mol����Ӧ�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ�����2��x=2mol��3mol�����x=3��
��x��ֵ��3��
��2������ȼ�ϵ���У�ͨ��������һ��Ϊ��Դ�ĸ�����ͨ��������һ��Ϊԭ��ص����������ڵ������Һ�ʼ��ԣ���a�缫��ӦʽΪ2H2-4e-+4OH-=4H2O����H2-2e-+2OH-=2H2O��������b�缫��ӦʽΪO2+4e-+2H2O=4OH-��
�ʴ�Ϊ��2H2-4e-+4OH-=4H2O����H2-2e-+2OH-=2H2O����
���������⿼�黯ѧƽ��ļ��㣬ԭ���ԭ�������͵缫��Ӧ��д��������Ŀ�ѶȲ���ע��Ի���֪ʶ�����⡢���ۣ�

��ϰ��ϵ�д�
 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д�
�����Ŀ
��2.5mol A��2.5mol B���ʢ���ݻ�Ϊ2L���ܱ�������������·�Ӧ��3A��g��+B��g��?x C��g��+2D��g������5s��Ӧ��ƽ�⣬�ڴ�5s��C��ƽ����Ӧ����Ϊ0.2mol?L-1?s-1��ͬʱ����1mol D�����������д�����ǣ�������
| A���ﵽƽ��״̬ʱA��ת����Ϊ50% |
| B��x=4 |
| C���ﵽƽ��״̬ʱ�����������ѹǿ����ʼʱѹǿ��Ϊ6��5 |
| D��5s��B�ķ�Ӧ����v��B��=0.05 mol/��L?s�� |
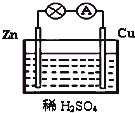 ��ͼΪԭ��ص�ʾ��ͼ����ش�
��ͼΪԭ��ص�ʾ��ͼ����ش�