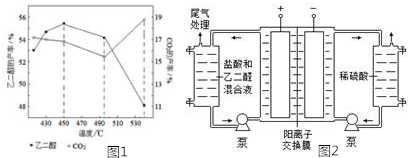
题目内容
20.工业上用双酚A来生产聚碳酸酯防碎塑料,欧盟认为含双酚A奶瓶会诱发性早熟,从2011年3月2日起,禁止生产含化学物质双酚A(BPA)的婴儿奶瓶.已知:双酚A的结构简式为
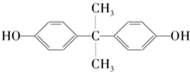 ,生产聚碳酸酯的过程如下:
,生产聚碳酸酯的过程如下: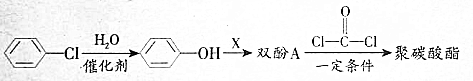
请回答下列问题:
(1)双酚A中含氧官能团的名称为羟基.
(2)有机物X为烃的含氧衍生物,其中含氧的质量分数为27.6%,经测定X的蒸气密度是同温同压下氢气的29倍,其核磁共振氢谱中只有1种峰,则X的结构简式为CH3COCH3.
(3)写出苯酚与X反应制取双酚A的化学方程式:
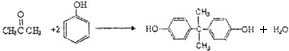 .
.
分析 氯苯发生水解反应生成苯酚,苯酚和X反应生成双酚A,有机物X为烃的含氧衍生物,经测定X的蒸气密度是同温同压下氢气的29倍,其相对分子质量为58,其核磁共振氢谱中只有1种峰,说明含有1种氢原子,其中含氧的质量分数为27.6%,则O原子个数=$\frac{58×27.6%}{16}$=1,C原子个数=$\frac{58-16×1}{12}$=3…6,所以X为CH3COCH3,双酚A和酰氯发生缩聚反应 生成聚碳酸酯,据此分析解答.
生成聚碳酸酯,据此分析解答.
解答 解:氯苯发生水解反应生成苯酚,苯酚和X反应生成双酚A,有机物X为烃的含氧衍生物,经测定X的蒸气密度是同温同压下氢气的29倍,其相对分子质量为58,其核磁共振氢谱中只有1种峰,说明含有1种氢原子,其中含氧的质量分数为27.6%,则O原子个数=$\frac{58×27.6%}{16}$=1,C原子个数=$\frac{58-16×1}{12}$=3…6,所以X为 ,双酚A和酰氯发生缩聚反应
,双酚A和酰氯发生缩聚反应 生成聚碳酸酯,
生成聚碳酸酯,
(1)双酚A中含氧官能团名称是羟基,故答案为:羟基;
(2)通过以上分析知,X为CH3COCH3,故答案为:CH3COCH3;
(3)苯酚与X反应制取双酚A,还生成水,该反应为 ,
,
故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,正确判断X结构简式是解本题关键,注意生成双酚A和生成聚碳酸酯时断键和成键位置,题目难度不大.

练习册系列答案
相关题目
10.下列实验操作或实验事故处理正确的是( )
| A. | 实验室制溴苯时,将苯与液溴混合后加到有铁丝的反应容器中 | |
| B. | 实验室制硝基苯时,将硝酸与苯混合后再滴加浓硫酸 | |
| C. | 实验时手指不小心沾上苯酚,立即用70℃以上的热水清洗 | |
| D. | 实验室检验卤代烃时,试剂只需用NaOH的水溶液和AgNO3溶液即可 |
11.下列关于元素周期表的说法正确的是( )
| A. | 过渡元素全部都是副族元素 | |
| B. | 短周期共有32 种元素 | |
| C. | 科学研究时,经常在过渡元素中寻找耐高温、耐腐蚀的合金材料 | |
| D. | 元素周期表共七个横行代表七个周期,18 个纵横代表18 个族 |
15.甲、乙、丙、丁、戊五种物质中,甲、乙、丙中均含有某种相同的元素,它们之间具有如右图所示转化关系(反应条件及部分产物已略去),下列有关物质的推断不正确的是( )


| A. | 假设:甲为Al(OH)3;结论:丁可能是盐酸 | |
| B. | 假设:甲为Na2CO3溶液;结论:戊可能是CO2 | |
| C. | 假设:甲为Fe;结论:丁可能是盐酸 | |
| D. | 假设:甲为N2;结论:戊可能是氧气 |
1. 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液(盛放于锥形瓶中)时,选择酚酞作指示剂,请填写下列空白:
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液(盛放于锥形瓶中)时,选择酚酞作指示剂,请填写下列空白:
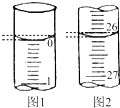
(1)滴定时一般左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶,直到加入最后一滴盐酸,溶液溶液颜色由红色变为无色,且半分钟内不变色,即达到滴定终点.若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸的体积为26.10 mL.
(2)某学生重复三次实验,记录数据如下表所示(待测NaOH溶液的体积均为25.00mL);
计算所测氢氧化钠溶液的物质的量浓度为0.1044 mol/L(保留四位小数)
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏高的是AC.
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管尖嘴处在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定开始时仰视读数,滴定结束时俯视读数.
 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液(盛放于锥形瓶中)时,选择酚酞作指示剂,请填写下列空白:
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液(盛放于锥形瓶中)时,选择酚酞作指示剂,请填写下列空白:(1)滴定时一般左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶,直到加入最后一滴盐酸,溶液溶液颜色由红色变为无色,且半分钟内不变色,即达到滴定终点.若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸的体积为26.10 mL.
(2)某学生重复三次实验,记录数据如下表所示(待测NaOH溶液的体积均为25.00mL);
| 滴定次数 | 0.1000mol-L-1盐酸的体积/mL | ||
| 滴定前 | 滴定后 | 体积/mL | |
| 1 | 0.10 | 26.21 | 26.11 |
| 2 | 1.56 | 31.30 | 29.74 |
| 3 | 0.22 | 26.31 | 26.09 |
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏高的是AC.
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管尖嘴处在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定开始时仰视读数,滴定结束时俯视读数.
8. Ⅰ:某学生用0.20mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
Ⅰ:某学生用0.20mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)①
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果偏小(填“偏大”、“偏小”或“无影响”)
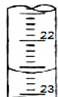
(3)右图是某次滴定时的滴定管中的液面,其读数为22.60mL
(4)根据下列数据:请计算待测盐酸溶液的浓度:0.2mol/L
Ⅱ按要求回答下列问题:
(5)某温度时,水的离子积常数KW=10-13,将此温度下pH=11的Ba(OH)2溶液aL与pH=1的H2SO4溶液bL混合,设混合溶液体积为两者之和,所得固体体积忽略不计.若所得混合溶液为中性,则a:b=10:1
(6)已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)=1.8×10-10,Ksp(AgY)=1.0×10-12,Ksp(AgZ)=8.7×10-17.则AgX、AgY、AgZ三者的溶解度(mol/L)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:s(AgX)>s(AgY)>s(AgZ);若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)减小(填“增大”“减小”或“不变”).
 Ⅰ:某学生用0.20mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
Ⅰ:某学生用0.20mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)①
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果偏小(填“偏大”、“偏小”或“无影响”)
(3)右图是某次滴定时的滴定管中的液面,其读数为22.60mL
(4)根据下列数据:请计算待测盐酸溶液的浓度:0.2mol/L
| 滴定次数 | 待测体积(ml) | 标准烧碱体积(ml) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
(5)某温度时,水的离子积常数KW=10-13,将此温度下pH=11的Ba(OH)2溶液aL与pH=1的H2SO4溶液bL混合,设混合溶液体积为两者之和,所得固体体积忽略不计.若所得混合溶液为中性,则a:b=10:1
(6)已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)=1.8×10-10,Ksp(AgY)=1.0×10-12,Ksp(AgZ)=8.7×10-17.则AgX、AgY、AgZ三者的溶解度(mol/L)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:s(AgX)>s(AgY)>s(AgZ);若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)减小(填“增大”“减小”或“不变”).
6.下列离子方程式正确的是( )
| A. | 二氧化锰和浓盐酸反应:MnO2+4H++4Cl-=Mn2++2Cl2↑+2H2O | |
| B. | 二氧化硅和氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O | |
| C. | 碳酸钡和稀硝酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | 铜和氯化铁溶液反应:Fe3++Cu=Fe2++Cu2+ |