题目内容
8.材料是人类赖以生存和发展的重要物质基础.①在下列材料中,属于无机非金属材料的是c(选填字母).
a.硬币 b.聚氯乙烯塑料 c.氮化硅陶瓷
②硅酸盐水泥是常用的建筑材料,它主要是以石灰石(碳酸钙或CaCO3)和黏土为原料制成.
③晶体硅是半导体材料,二氧化硅是光纤的主要成分,晶体硅和二氧化硅都属于原子(选填“离子”、“分子”或“原子”)晶体.
④橡胶是制造轮胎的重要原料,天然橡胶通过硫化处理,使它的分子转化为体型网状结构结构,从而增大橡胶的强度.
⑤钢铁的生产与使用是人类文明和生活进步的一个重要标志.工业炼铁原理的主要化学反应方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.钢铁的腐蚀主要是由电化学腐蚀造成的.金属腐蚀会造成巨大的经济损失,钢铁在潮湿的空气中因发生电化学反应更容易被腐蚀,其负极反应式为Fe-2e-═Fe2+.
分析 ①硬币材料为合金,聚氯乙烯属于有机合成分子材料;
②硅酸盐水泥主要是以石灰石和黏土为原料;
③晶体硅和二氧化硅都属于原子晶体;
④天然橡胶通过硫化处理,使它的分子转化为体型网状结构,从而增大橡胶的强度;
⑤工业炼铁原理为CO与氧化铁反应生成Fe与二氧化碳;钢铁的腐蚀主要是由电化学腐蚀造成的;负极上铁失电子发生氧化反应.
解答 解:①硬币材料为合金,聚氯乙烯属于有机合成分子材料,氮化硅陶瓷属于无机非金属性材料,故答案为:c;
②硅酸盐水泥主要是以石灰石和黏土为原料高温烧制而成,故答案为:石灰石;
③晶体硅和二氧化硅都是通过共价键形成的空间立体网状结构,属于原子晶体,故答案为:原子;
④天然橡胶通过硫化处理,使它的分子转化为体型网状结构,从而增大橡胶的强度,故答案为:体型网状结构;
⑤工业炼铁原理为CO与氧化铁反应生成Fe与二氧化碳,方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
钢铁有化学腐蚀与电化学腐蚀,但主要是由电化学腐蚀造成的;
负极上铁失电子发生氧化反应,电极反应式为Fe-2e-=Fe2+,
故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;电化学;将铁钉用蒸馏水洗涤后放入硫酸铜溶液中,若表面无红色物质生成,说明发蓝后铁钉的表面有一层致密的氧化膜.
点评 本题考查化学与生活,题目比较综合,涉及环境污染、无机非金属材料、营养平衡与人体健康等,难度不大,注意对基础知识的全面掌握.

练习册系列答案
相关题目
18.符合如图阴影部分的物质是( )
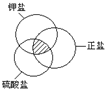

| A. | KHSO4 | B. | K2SO4 | C. | K2CO3 | D. | KAl(SO4)2•12H2O |
19.可逆反应mA(s)+nB(g)?cC(g)+dD(g) 反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )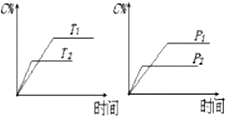

| A. | 达平衡后,加入催化剂则C%增大 | B. | 达平衡后,若升温,平衡左移 | ||
| C. | 化学方程式中n>c+d | D. | 达平衡后,增加A的量平衡向右移动 |
3.世界上60%的镁是从海水中提取的,其主要步骤如下:
①把贝壳制成石灰乳
②在海水中加入石灰乳,过滤,洗涤沉淀物
③将沉淀物与盐酸反应,结晶、过滤
④在氯化氢热气流中干燥晶体
⑤电解上述晶体的熔融物.
下列说法正确的是( )
①把贝壳制成石灰乳
②在海水中加入石灰乳,过滤,洗涤沉淀物
③将沉淀物与盐酸反应,结晶、过滤
④在氯化氢热气流中干燥晶体
⑤电解上述晶体的熔融物.
下列说法正确的是( )
| A. | 镁元素在元素周期表中位于第三周期、第ⅡB族 | |
| B. | 第②步洗涤完毕后向洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净 | |
| C. | 在工业生产上可用NaOH溶液代替石灰乳 | |
| D. | 步骤⑤也可以采用电解该晶体水溶液的方法 |
13.25℃时,向盛有50mL pH=3的HA溶液的绝热容器中加入pH=14的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )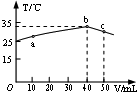

| A. | HA溶液的物质的量浓度为0.01mol/L | |
| B. | a→b的过程中,混合溶液中可能存在:c(A-)=c(Na+) | |
| C. | b→c的过程中,温度降低的主要原因是溶液中A-发生了水解反应 | |
| D. | 25℃时,HA的电离平衡常数K约为1.25×10-3 |
13.硫化碱法是工业上制备Na2S2O3的方法之一,反应原理为:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2(该反应△H>0)某研究小组在实验室用硫化碱法制备Na2S2O3•5H2O流程如下.
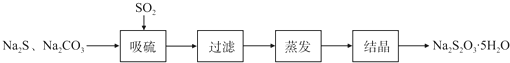
(1)吸硫装置如图所示.
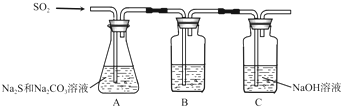
①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是品红、溴水或KMnO4溶液,表明SO2吸收效率低的实验现象是B中溶液颜色很快褪色;
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是控制SO2的流速、适当升高温度.(写出两条)
(2)假设本实验所用的Na2CO3含少量NaCl、NaOH,设计实验方案进行检验.(室温时CaCO3饱和溶液的pH=10.2)
限选试剂及仪器:稀硝酸、AgNO3溶液、CaCl2溶液、Ca(NO3)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管
(3)Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:准确称取a g KIO3(化学式量:214)固体配成溶液,加入过量KI固体和H2SO4溶液,滴加指示剂,用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为V mL.则c(Na2S2O3)=$\frac{6000a}{214V}$mol•L-1.(只列出算式,不作运算)
已知:Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O 2S2O32-+I2═S4O62-+2I-.

(1)吸硫装置如图所示.

①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是品红、溴水或KMnO4溶液,表明SO2吸收效率低的实验现象是B中溶液颜色很快褪色;
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是控制SO2的流速、适当升高温度.(写出两条)
(2)假设本实验所用的Na2CO3含少量NaCl、NaOH,设计实验方案进行检验.(室温时CaCO3饱和溶液的pH=10.2)
限选试剂及仪器:稀硝酸、AgNO3溶液、CaCl2溶液、Ca(NO3)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管
| 序号 | 实验操作 | 预期现象 | 结论 |
| ① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解,滴加足量稀硝酸,再滴加少量AgNO3溶液,振荡. | 有白色沉淀生成 | 样品含NaCl |
| ② | 另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解,另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解,加入过量CaCl2溶液,搅拌,静置,用pH计测定上层清液pH | 有白色沉淀生成,上层清液pH大于10.2 | 样品含NaOH |
已知:Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O 2S2O32-+I2═S4O62-+2I-.
14.下列属于氧化物的是( )
| A. | NaCl | B. | MgO | C. | H2SO4 | D. | NaOH |
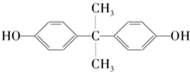 ,生产聚碳酸酯的过程如下:
,生产聚碳酸酯的过程如下: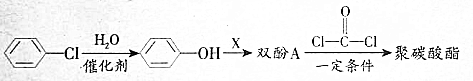
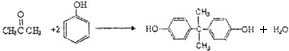 .
.