题目内容
12.下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是( )| 编号 | 化学反应 | 离子方程式 | 评价 |
| ① | 碳酸钙与醋酸反应 | CO32-+2CH3COOH=CO2↑+H2O+2CH3COO- | 错误,碳酸钙是弱电解质,不应写成离子形式 |
| ② | 氢氧化钠溶液中通入CO2 | OH-+CO2=HCO3- | 错误,通往过量CO2应生成CO32- |
| ③ | NaHCO3的水解 | HCO3-+H2O?H2CO3+OH- | 正确 |
| ④ | 等物质的量的FeBr2和Cl2反应 | 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | 正确 |
| A. | ①③ | B. | ③④ | C. | ②③ | D. | ①④ |
分析 ①碳酸钙在离子反应中保留化学式,为强电解质;
②足量二氧化碳反应生成HCO3-,少量二氧化碳反应生成CO32-;
③水解生成碳酸和NaOH,为可逆反应;
④等物质的量的FeBr2和Cl2反应,由电子守恒可知,亚铁离子全部被氧化,溴离子一半被氧化.
解答 解:①碳酸钙与醋酸反应的离子反应为CaCO3+2CH3COOH=Ca2++CO2↑+H2O+2CH3COO-,碳酸钙为强电解质,故错误;
②氢氧化钠溶液中通入过量CO2的离子的反应为OH-+CO2=HCO3-,故错误;
③NaHCO3的水解离子反应为HCO3-+H2O?H2CO3+OH-,故正确;
④等物质的量的FeBr2和Cl2反应的离子反应为2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-,故正确;
故选B.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应、水解反应的判断,题目难度不大.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
7.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| B. | 标准状况下,11.2L苯中含有分子的数目为0.5NA | |
| C. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| D. | 物质的量浓度为1mol/L100mlHCl溶液中含0.1molHCl分子 |
9.甲图和乙图分别是1s电子的概率分布图和原子轨道图.下列有关说法正确的是( )

| A. | 甲图中的小黑点疏密表述电子在核外空间出现机会的大小 | |
| B. | 甲图中的每个小黑点表示1个电子 | |
| C. | 乙图表示1s电子只能在球体内出现 | |
| D. | 乙图表明1s轨道呈圆形,有无数对称轴 |
10.如图装置可用来收集下列某种气体,该气体是( )
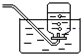

| A. | SO2 | B. | Cl2 | C. | O2 | D. | HCl |
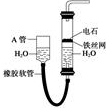 用图中的实验装置制取乙炔.
用图中的实验装置制取乙炔.