题目内容
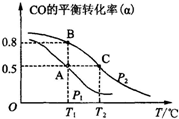
13.运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义(1)硫酸生产中,SO2催化氧化生成SO3; 2SO2(g)+O2(g)?2SO3(g),平衡时,混合体系中SO3的百分含量和温度的关系如图1所示.根据图示回答下列问题:
①2SO2(g)+O2(g)?2SO3(g)的△H<0(填“>”或“<”);若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡向左移动(填“向左”“向右”或“不移动”)
②若温度为T1、T2,反应的平衡常数分别为K1,K2,则K1>K2;温度为T1时,反应进行到状态D时,v 正>v逆(填“>”“<”或“=”)
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,
①如图2是一定的温度和压强下N2(g)和H2(g)反应生成lmol NH3(g)过程中能量变化示意图,图中E1、E2分别表示的意义是正反应的活化能、逆反应的活化能
②请写出工业合成氨的热化学方程式:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=(Q1-Q2)kJ/mol(△H的数值用含字母Q1、Q2的代数式表示)
分析 (1)①根据温度对化学平衡的影响结合图象分析该反应是放热反应还是吸热反应;
②根据T1的T2关系结合图象分析平衡的移动,根据反应物和生成物物质的量的改变引起化学平衡常数的改变判断K1、K2的关系;根据图象中曲线及曲线上、下方区域表示的含义分析,曲线表示平衡状态,曲线下方表示向正反应方向进行,曲线上方表示向逆反应方向进行;
(2)①根据能量变化示意图中能量数据的含义来回答;
②由图甲可知,N2和H2反应生成1molNH3放出的热量为(Q2-Q1)kJ,注明物质的聚集状态与反应热书写热化学方程式.
解答 解:(1)①根据图象可知:升高温度,SO3的平衡含量减少,说明升高温度,平衡向逆反应方向移动.根据平衡移动原理:升高温度,平衡向吸热反应方向移动,因此2SO2(g)+O2(g)?2SO3(g)的正反应是放热反应,△H<0;若在恒温、恒压条件下向上述平衡体系中通入氦气,则容器的容积扩大,物质的浓度减小,容器内气体的压强减小,平衡向气体体积增大的方向移动,因此平衡逆向移动.即向左移动,故答案为:<;向左;
②由于升高温度,平衡逆向移动,所以若温度为T1、T2,反应的平衡常数分别为K1,K2,则K1>K2;温度为T1时,反应进行到状态D时,未达到平衡时的SO3的浓度,所以反应正向进行,则v 正>v逆,故答案为:>;>;
(2)图示是一定的温度和压强下N2(g)和H2(g)反应生成lmol NH3(g)过程中能量变化示意图,图中E1 表示的是正反应的活化能(或正反应发生需要的最低能量);E2表示的意义是E2:逆反应的活化能(或逆反应发生需要的最低能量),
故答案为:正反应的活化能;逆反应的活化能;
②根据图示可知每产生1mol NH3(g)放出能量是(Q2-Q1)kJ,因此工业合成氨的热化学方程式是$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=(Q1-Q2)kJ/mol,
故答案为:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=(Q1-Q2)kJ/mol.
点评 本题综合考查化学平衡的影响因素,化学平衡的计算与判断,为高考常见题型和高频考点,注意把握图象的分析与判断,本题还要注意反应热与焓变,把握活化能与反应热的关系,难度不大.

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案| A. | Na2O2与Na2O | B. | Na2O2 | C. | Na2O2与Na | D. | Na和Na2O |
(1)请帮助他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、碘化钾、淀粉溶液
实验记录:
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为黄色 | 2Fe2++Cl2=2Fe3++2Cl- | Fe2+具有还原性 |
| ② | 在FeCl2溶液中加入锌片 | (不写) | Zn+Fe2+=Zn2++Fe | Fe2+具有氧化性 |
| ③ | 在FeCl3溶液中加入足量铁粉 | 溶液由黄色变为浅绿色 | Fe+2Fe3+=3Fe2+ | Fe3+具有氧化性 |
| ④ | 在FeCl3溶液中滴入适量KI溶液和淀粉溶液 | 变蓝色 | 2Fe3++2I-=2Fe2++I2 | Fe3+具有氧化性 |
(2)亚铁盐在溶液中易被氧化,而实验中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时如何防止亚铁盐被氧化加铁粉.
(3)检验某铁盐溶液中是否含有亚铁盐的方法是取少量溶液于试管中滴加1滴酸性KMnO4溶液,若紫色褪去,则有Fe2+.
时间s 浓度mol/L | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
(1)该反应达到平衡时,四氧化二氮的转化率为60%,表中c2>c3(填“>”、“<”或“=”).
(2)20s时四氧化二氮的浓度c1=0.070mol/L,在0s~20s时间段内,四氧化二氮的平均反应速率为0.0015mol/(L•s).
(3)100℃时,该反应的平衡常数K=0.36mol/L.
(4)若在相同情况下最初向该容器中充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是0.200mol/L.
(5)若在相同情况下向该容器中充入0.2mol四氧化二氮和0.3mol二氧化氮气体,则到达平衡前v(正)> v(逆)(填“>”、“<”或“=”).
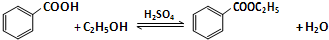
已知:
| 物质 | 颜色状态 | 密度/g/cm3 | 熔点/℃ | 沸点/℃ |
| 苯甲酸 | 白色固体 | 1.2659 | 122 | 249 |
| 苯甲酸乙酯 | 无色液体 | 1.05 | -34.6 | 212.6 |
| 乙酸 | 无色液体 | 1.0492 | 16.6 | 117.9 |
| 乙醇 | 无色液体 | 0.789 | -117.3 | 78.5 |
| 乙酸乙酯 | 无色液体 | 0.894-0.898 | -83.6 | 77.1 |
| 乙醚 | 无色液体 | 0.713 | -116.3 | 34.6 |
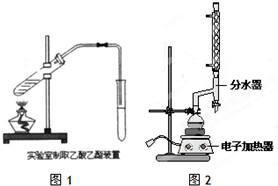
(1)如图1为课本上制取乙酸乙酯的实验装置图,请回答下列问题:
①乙醇、乙酸和浓硫酸混合的先后顺序先加乙醇,再加浓硫酸,等冷却再加乙酸;
②浓硫酸的作用是催化剂和吸水剂;
③实验开始前在饱和碳酸钠加入酚酞,溶液会变红,随着乙酸乙酯的蒸出,红色会变浅,但是无气体产生,请写出发生该变化的离子反应方程式CH3COOH+CO32-=CH3COO-+HCO3-;
(2)按照图2所示装置制备苯甲酸乙酯.
①制备:在圆底烧瓶中加入12.20g苯甲酸、25mL乙醇(过量)、4mL浓硫酸,混合均匀并加入沸石,按图2所示连接好仪器,其中分水器的作用是分离出反应生成的水,控制温度加热回流2h.
a.实验中使用分水器不断分离除去水的目的是分离反应过程中生的水,促进酯化反应向正反应方向进行;
b.从提供的分析实验室制取苯甲酸乙酯为什么不使用制取乙酸乙酯一样的装置?如果使用制取乙酸乙酯的装置,会使乙醇大量蒸馏出去,实验效率大大降低;
②产品的提纯
将圆底烧瓶中的残液倒入盛有冷水的烧瓶中,分批加入Na2CO3溶液呈中性;用分液漏斗分出有机层得粗产品.水层用25mL乙醚萃取分液,醚层与粗产品合并;在粗产品加入无水氯化钙后,静置、过滤,过滤液进行蒸馏,蒸出乙醚后,继续升温,接收210~213℃的馏分;产品经检验合格,测得产品体积为6mL.
c.在该实验分液过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”可“下口倒出”);
d.该实验中苯甲酸乙酯的产率为42%;
e.若加入的Na2CO3溶液不足,在之后的蒸馏时烧瓶内会出现白烟生成,产生该现象的原因在苯甲酸乙酯中有未除净的苯甲酸,受热至100℃时升华.
 空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.
空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.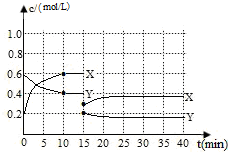 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物浓度随时间变化关系如下图所示.X与Y两条曲线中,Y表示N2O4浓度随时间的变化
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物浓度随时间变化关系如下图所示.X与Y两条曲线中,Y表示N2O4浓度随时间的变化