题目内容
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、1molNa2O和Na2O2混合物中含阴离子的总数为NA |
| B、标准状况下,22.4 LCCl4含CCl4分子为NA |
| C、1mol H3O+含质子数为10 NA |
| D、1 L0.1 mol?L-1的CuCl2溶液中含Cu2+为0.1NA |
考点:阿伏加德罗常数
专题:
分析:A、Na2O和Na2O2均由两个阳离子和一个阴离子构成;
B、标况下,CCl4是液态;
C、根据 H3O+含有的质子数来分析;
D、Cu2+是弱碱阳离子,在水溶液中会水解.
B、标况下,CCl4是液态;
C、根据 H3O+含有的质子数来分析;
D、Cu2+是弱碱阳离子,在水溶液中会水解.
解答:
解:A、Na2O和Na2O2均由两个阳离子和一个阴离子构成,故1molNa2O和Na2O2混合物中含阴离子的总数为NA,故A正确;
B、标况下,CCl4是液态,故B错误;
C、1molH3O+含11mol质子,故C错误;
D、Cu2+是弱碱阳离子,在水溶液中会水解,故1 L0.1 mol?L-1的CuCl2溶液中含Cu2+少于0.1NA,故D错误.
故选A.
B、标况下,CCl4是液态,故B错误;
C、1molH3O+含11mol质子,故C错误;
D、Cu2+是弱碱阳离子,在水溶液中会水解,故1 L0.1 mol?L-1的CuCl2溶液中含Cu2+少于0.1NA,故D错误.
故选A.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
工业上常用焦炭和二氧化硅在电炉中发生反应制取粗硅,化学方程式;SiO2+2C
Si+2CO.下列说法不正确的是( )
| ||
| A、该反应属于置换反应 |
| B、C是还原剂,发生还原反应 |
| C、SiO2是氧化剂,在反应中还原 |
| D、氧化还原反应的实质是电子的转移 |
N2O俗称“笑气”,曾用作可吸入性麻醉剂.用以下反应可制取N2O:CO+NO2→CO2+N2O.下列说法正确的是( )
| A、反应中每生成1 mol N2O,消耗1.5 mol CO |
| B、等物质的量的N2O和CO2含有相等的电子数 |
| C、N2O只具有氧化性,无还原性 |
| D、反应中每生成1 mol N2O,电子转移的物质的量为3 mol |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A、HClO的结构式:H-Cl-O | ||
B、Na2O2的电子式: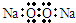 | ||
C、中子数为20的氯原子:
| ||
D、铝原子的结构示意图 |
以下物质是强电解质的是( )
| A、BaSO4 |
| B、浓H2SO4 |
| C、盐酸 |
| D、NH3 |
已知化学反应2C(s)+O2(g)═2CO(g),2CO(g)+O2(g)=2CO2(g)都是放热反应.据此判断,下列说法中不正确的是( )
| A、1.2gC所具有的能量一定高于28gCO所具有的能量 |
| B、56g CO和32g O2所具有的总能量大于88g CO2所具有的总能量 |
| C、12g C和32g O2所具有的总能量大于44g CO2所具有的总能量 |
| D、将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |