题目内容
5.下列有关实验原理或操作不正确的是( )| A. |  实验室制NH3 | B. | 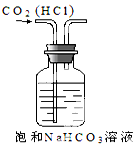 除去CO2中的HCl | C. |  检验K2CO3中的K+ | D. | 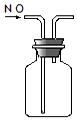 收集NO气体 |
分析 A.氯化铵与氢氧化钙加热生成氨气,氨气的密度比空气的密度小;
B.HCl与碳酸氢钠反应生成二氧化碳;
C.观察K的焰色反应透过蓝色的钴玻璃;
D.NO不能利用排空气法收集,易被氧化.
解答 解:A.氯化铵与氢氧化钙加热生成氨气,氨气的密度比空气的密度小,向下排空气法收集,试管口塞一团棉花防止与空气对流,故A正确;
B.HCl与碳酸氢钠反应生成二氧化碳,图中导管长进短出可除杂,故B正确;
C.观察K的焰色反应透过蓝色的钴玻璃,图中操作合理,故C正确;
D.NO不能利用排空气法收集,易被氧化,应选排水法收集,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的制备、混合物分离提纯、焰色反应为解答的关键,侧重分析与实验能力的考查,注意元素化合物与实验的结合,题目难度不大.

练习册系列答案
相关题目
15.在一密闭容器中,反应aX(g)+bY(g)?cZ(g)达到平衡时的平衡常数为K1;在温度不变的条件下将容器体积压缩至原来的一半,达到新的平衡后Y的浓度为原来的1.6倍,平衡常数为K2.则K1 与K2的大小关系( )
| A. | K1=K2 | B. | K1<K2 | C. | K1>K2 | D. | 无法确定 |
16.下列关于 ${\;}_{8}^{17}O$的说法正确的是( )
| A. | ${\;}_{8}^{17}O$原子核内含有8个中子 | B. | ${\;}_{8}^{17}O$原子核内含有8个质子 | ||
| C. | ${\;}_{8}^{17}O$原子核外有17个电子 | D. | ${\;}_{8}^{17}O$原子核内含有17个质子 |
20.硅单质及其化合物应用范围很广.请回答下列问题
(1)制备硅半导体材料必须先得到高纯硅的主要方法,其生产过程示意图如图所示.
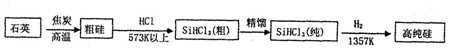
①写出由纯SiHCl3制备高纯硅的化学反应方程式SiHCl3+H2$\frac{\underline{\;1357K\;}}{\;}$Si+3HCl
②整个制备过程必须严格控制无水无氧.SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式,H2还原SiHCl3过程中若混入O2,可能引起的后果是高温下,H2遇O2发生爆炸.
(2)硅酸钠水溶液俗称水玻璃.取少量硅酸钠溶液于试管中,逐滴加入饱和氯化铵溶液,振荡.写出实验现象其产生原因:生成白色絮状沉淀,又刺激性气味的气体生成,SiO32-与NH4+发生双水解反应,生成氨气和硅酸沉淀.
①2O2(g)+N2(g)=N2O4,(l)△H1
②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2 H4 (1)+N2O4 (1)=3N2 (g)+4H2O(g)△H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=2△H3-2△H2-△H1,联氨和N2O4可作为火箭助推剂,折算在标准状况下的数据,燃爆后气体的体积与燃爆前的体积之比为:1228.6.
(4)联氨为二元弱減,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为(已知:N2H4+H+?N2H5+的K=8.7×107;KW=1.0×10-14),.联氨与硫酸形成的酸式盐的化学式为N2H6(HSO4)2.
(5)联氨是一种常用的还原剂.向装有少量AgBr的试管中加入联氨溶液,观察到的现象是固体逐渐变黑,并有气泡产生.联氨可用于处理锅炉水中的氧;防止锅炉被腐蚀,理论上1kg的联氨可除去水中溶解的O21 kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是N2H4的用量少,不产生其他杂质(反应产物为N2和H2O),而Na2SO3产生Na2SO4.
(1)制备硅半导体材料必须先得到高纯硅的主要方法,其生产过程示意图如图所示.

①写出由纯SiHCl3制备高纯硅的化学反应方程式SiHCl3+H2$\frac{\underline{\;1357K\;}}{\;}$Si+3HCl
②整个制备过程必须严格控制无水无氧.SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式,H2还原SiHCl3过程中若混入O2,可能引起的后果是高温下,H2遇O2发生爆炸.
(2)硅酸钠水溶液俗称水玻璃.取少量硅酸钠溶液于试管中,逐滴加入饱和氯化铵溶液,振荡.写出实验现象其产生原因:生成白色絮状沉淀,又刺激性气味的气体生成,SiO32-与NH4+发生双水解反应,生成氨气和硅酸沉淀.
①2O2(g)+N2(g)=N2O4,(l)△H1
②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2 H4 (1)+N2O4 (1)=3N2 (g)+4H2O(g)△H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=2△H3-2△H2-△H1,联氨和N2O4可作为火箭助推剂,折算在标准状况下的数据,燃爆后气体的体积与燃爆前的体积之比为:1228.6.
| N2H4 | N2O4 | |
| 密度/g/cm3 | 1.004 | 1.44 |
(5)联氨是一种常用的还原剂.向装有少量AgBr的试管中加入联氨溶液,观察到的现象是固体逐渐变黑,并有气泡产生.联氨可用于处理锅炉水中的氧;防止锅炉被腐蚀,理论上1kg的联氨可除去水中溶解的O21 kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是N2H4的用量少,不产生其他杂质(反应产物为N2和H2O),而Na2SO3产生Na2SO4.
10.如图,各烧杯中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )
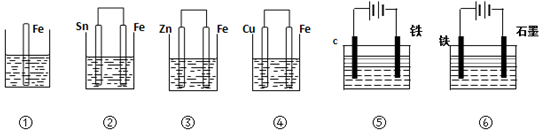

| A. | ④>②>①>③>⑤>⑥ | B. | ⑥>④>②>①>③>⑤ | C. | ④>②>⑤>③>⑥>① | D. | ⑥>③>②>④>①>⑤ |
12. 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在.
(1)某研究小组设计了制备Na2S2O3•5H2O的装置和部分操作步骤如下.
Ⅰ.打开Kl,并闭K2,向圆底烧瓶中加人足量浓硫酸,加热.
Ⅱ.C中的混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近7时即停止C中的反应.
Ⅲ.过滤C中的混合液.
Ⅳ.将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
①Ⅰ中,圆底烧瓶中发生反应的化学方程式是:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
②Ⅱ中“停止C中的反应”的操作是打开K2,关闭K1.
③Ⅳ中将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.Na2S2O3•5H2O的溶解度随温度升高显著增大,所得产品通过重结晶方法提纯.
④装置B的作用是在C中的反应停止后吸收A中产生的多余SO2防止空气污染.
(2)依据反应2S2O32-+I2═S4O62-+2I-,可用I2的标准溶液测定产品的纯度.取5.5g产品,配制成100mL溶液.取10mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol•L-1I2的标准溶液进行滴定,相关数据记录如下表所示.
①判断达到滴定终点的现象是加入最后一滴I2标准溶液后,溶液变蓝,且半分钟内颜色不改变.
②Na2S2O3•5H2O在产品中的质量分数是90.2%(Na2S2O3•5H2O的式量为248,计算结果保留1位小数).
 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在.(1)某研究小组设计了制备Na2S2O3•5H2O的装置和部分操作步骤如下.
Ⅰ.打开Kl,并闭K2,向圆底烧瓶中加人足量浓硫酸,加热.
Ⅱ.C中的混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少.当C中溶液的pH接近7时即停止C中的反应.
Ⅲ.过滤C中的混合液.
Ⅳ.将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.
①Ⅰ中,圆底烧瓶中发生反应的化学方程式是:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
②Ⅱ中“停止C中的反应”的操作是打开K2,关闭K1.
③Ⅳ中将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品.Na2S2O3•5H2O的溶解度随温度升高显著增大,所得产品通过重结晶方法提纯.
④装置B的作用是在C中的反应停止后吸收A中产生的多余SO2防止空气污染.
(2)依据反应2S2O32-+I2═S4O62-+2I-,可用I2的标准溶液测定产品的纯度.取5.5g产品,配制成100mL溶液.取10mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol•L-1I2的标准溶液进行滴定,相关数据记录如下表所示.
| 编号 | 1 | 2 | 3 | 4 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 17.13 | 20.03 |
②Na2S2O3•5H2O在产品中的质量分数是90.2%(Na2S2O3•5H2O的式量为248,计算结果保留1位小数).
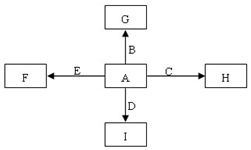 图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G$\stackrel{高温}{→}$B+H能放出大量的热,该反应曾应用于铁轨的焊接;
图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:①反应C+G$\stackrel{高温}{→}$B+H能放出大量的热,该反应曾应用于铁轨的焊接; ,它的空间构型是直线型;
,它的空间构型是直线型;