题目内容
16.下列关于 ${\;}_{8}^{17}O$的说法正确的是( )| A. | ${\;}_{8}^{17}O$原子核内含有8个中子 | B. | ${\;}_{8}^{17}O$原子核内含有8个质子 | ||
| C. | ${\;}_{8}^{17}O$原子核外有17个电子 | D. | ${\;}_{8}^{17}O$原子核内含有17个质子 |
分析 原子的质量数标在左上角,质子数标在左下角,而且质量数=质子数+中子数,原子的质子数=电子数=核电荷数=原子序数,据此分析.
解答 解:178O的质子数为8,根据原子的质子数=电子数=核电荷数=原子序数,故其电子数也为8.而17为其质量数,故中子数N=17-8=9.
A、178O的中子数为9,故A错误;
B、178O的质子数为8,故B正确;
C、178O的电子数为8,故C错误;
D、178O的质子数为8,故D错误.
故选B.
点评 本题考查了在原子结构中质子数、中子数和质量数之间的关系,难度不大,应注意的是原子的质子数=电子数=核电荷数=原子序数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.已知:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98kJ/mol.某温度下,向一体积为2L的密闭容器中充入0.2mol SO2和0.1mol O2,1min后达到平衡,压强变为原来的80%,下列说法不正确的是( )
| A. | 1min内用O2表示的反应速率为0.03 mol•L-1•min-1 | |
| B. | 该反应的平衡常数数值为7.5 | |
| C. | SO2的平衡转化率为60% | |
| D. | 降低温度,SO2平衡浓度减小 |
11.用标准浓度的NaOH溶液滴定未知浓度的盐酸时下列情况会使盐酸物质的量浓度偏低的是( )
| A. | 碱式滴定管用蒸馏水洗净后,直接注入标准浓度的NaOH溶液 | |
| B. | 碱式滴定管尖端有气泡,滴定后气泡消失 | |
| C. | 记录消耗的碱液,滴定前平视,滴定后俯视凹液面 | |
| D. | 锥形瓶用蒸馏水洗净后,直接装入未知浓度的盐酸 |
5.下列有关实验原理或操作不正确的是( )
| A. |  实验室制NH3 | B. | 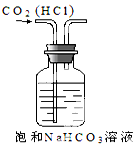 除去CO2中的HCl | C. |  检验K2CO3中的K+ | D. | 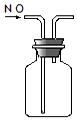 收集NO气体 |
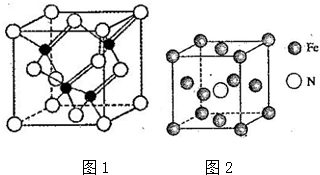
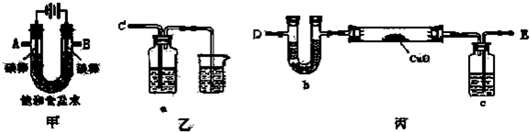
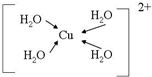 (配位键用→标出).
(配位键用→标出).