题目内容
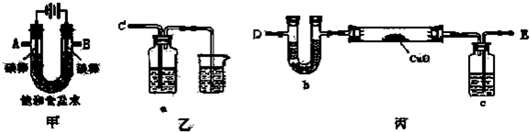
14.现有A、B、C、D四瓶溶液,分别是H2SO4、BaCl2、Na2SO4、Na2CO3中的一种.根据以下实验及现象回答下列问题:①A加入B中无反应 ②A加入C中有气体产生 ③D加入A中有沉淀产生.
(1)请写出四瓶溶液中物质的化学式:AH2SO4;BNa2SO4.
(2)写出A与C反应的离子方程式:2H++CO32-=CO2↑+H2O.A与D反应的离子方程式:Ba2++SO42-=BaSO4↓.
分析 A加入C中有气体产生,则A、C为H2SO4、Na2CO3中的一种,BaCl2与H2SO4、Na2SO4、Na2CO3反应均生成白色沉淀,结合D加入A中有沉淀产生,可知D为BaCl2,A加入B中无反应,则A为H2SO4,B为Na2SO4,以此来解答.
解答 解:A加入C中有气体产生,则A、C为H2SO4、Na2CO3中的一种,BaCl2与H2SO4、Na2SO4、Na2CO3反应均生成白色沉淀,结合D加入A中有沉淀产生,可知D为BaCl2,A加入B中无反应,则A为H2SO4,B为Na2SO4,C为Na2CO3,
(1)由上述分析可知,A为H2SO4,B为Na2SO4,故答案为:H2SO4;Na2SO4;
(2)A与C反应的离子方程式为2H++CO32-=CO2↑+H2O,A与D反应的离子方程式为Ba2++SO42-=BaSO4↓,
故答案为:2H++CO32-=CO2↑+H2O;Ba2++SO42-=BaSO4↓.
点评 本题考查无机物的推断,为高频考点,把握A与C生成气体、A与D生成沉淀为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
相关题目
5.下列有关实验原理或操作不正确的是( )
| A. |  实验室制NH3 | B. | 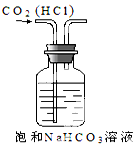 除去CO2中的HCl | C. |  检验K2CO3中的K+ | D. | 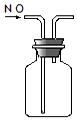 收集NO气体 |
2.在物质结构研究的历史上,首先提出原子结构有核模型的科学家是( )
| A. | 汤姆生 | B. | 玻尔 | C. | 卢瑟福 | D. | 普朗克 |
9.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下,8gO2含有4NA个电子 | |
| B. | 任意条件下,16g O3所含的原子数为NA | |
| C. | 由CH4和C2H6组成的混合物中共有NA个分子,其中的氢原子数为5NA | |
| D. | 46 g二氧化氮和46 g四氧化二氮含有的原子数均是6NA |
19.下列关于物质分类的说法正确的是( )
①稀豆浆、硅酸、氯化铁溶液都属于胶体
②HF、HI都属于弱电解质
③Na2O、MgO、Al2O3均属于碱性氧化物
④明矾、冰醋酸、四氧化三铁都不是混合物
⑤葡萄糖、油脂都不属于有机高分子化合物.
①稀豆浆、硅酸、氯化铁溶液都属于胶体
②HF、HI都属于弱电解质
③Na2O、MgO、Al2O3均属于碱性氧化物
④明矾、冰醋酸、四氧化三铁都不是混合物
⑤葡萄糖、油脂都不属于有机高分子化合物.
| A. | ④⑤ | B. | ②④ | C. | ①② | D. | ③⑤ |
3.下列说法正确的是( )
| A. | 乙烯和甲烷都能发生加成反应 | |
| B. | 煤焦油、石油、花生油都属于烃 | |
| C. | 甲烷、乙烯、苯都可通过石油分馏得到 | |
| D. |  + + $\stackrel{△}{→}$ $\stackrel{△}{→}$ 反应属于加成反应 反应属于加成反应 |
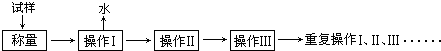
1.测定硫酸铜晶体(CuSO4•xH2O)结晶水含量的实验流程如下:
回答下列问题:
(1)以下是实验中可能用到的几种仪器,请在图下方横线上写出仪器名称.
a. 电子天平 b.
电子天平 b. 坩埚 c.
坩埚 c.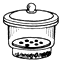 干燥器 d.
干燥器 d.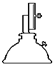 酒精喷灯
酒精喷灯
①“操作I”是灼烧硫酸铜晶体,用到上述bd(填序号)仪器.
②“操作Ⅱ”的操作是冷却,必须在c(填序号)中进行.
(2)“重复操作Ⅰ、Ⅱ、Ⅲ”,称为恒重操作.
判断达到恒重的依据是相邻两次称量的质量差小于0.001g;
进行恒重操作的目的是确保晶体失去全部结晶水.
(3)某学生实验后得到以表数据:
①根据以上数据计算该硫酸铜晶体中结晶水x的值为5.2(精确到0.1).
②该学生测定结果偏高(填“偏高”、“偏低”或“正确”).
③从下列分析中选出该学生产生实验误差的原因可能是(填序号)c.
a.没有进行恒重操作
b.加热固体到白色后,露置在空气中冷却
c.加热过程中晶体有少量溅失
d.加热后在干燥器中冷却至室温后称量.

回答下列问题:
(1)以下是实验中可能用到的几种仪器,请在图下方横线上写出仪器名称.
a.
 电子天平 b.
电子天平 b. 坩埚 c.
坩埚 c. 干燥器 d.
干燥器 d. 酒精喷灯
酒精喷灯①“操作I”是灼烧硫酸铜晶体,用到上述bd(填序号)仪器.
②“操作Ⅱ”的操作是冷却,必须在c(填序号)中进行.
(2)“重复操作Ⅰ、Ⅱ、Ⅲ”,称为恒重操作.
判断达到恒重的依据是相邻两次称量的质量差小于0.001g;
进行恒重操作的目的是确保晶体失去全部结晶水.
(3)某学生实验后得到以表数据:
| 加热前质量 | 加热后质量 | |
| m1(容器) | m2(容器+晶体) | m3(容器+无水硫酸铜) |
| 5.200g | 7.900g | 6.900g |
②该学生测定结果偏高(填“偏高”、“偏低”或“正确”).
③从下列分析中选出该学生产生实验误差的原因可能是(填序号)c.
a.没有进行恒重操作
b.加热固体到白色后,露置在空气中冷却
c.加热过程中晶体有少量溅失
d.加热后在干燥器中冷却至室温后称量.