题目内容
20.实验室要配制1.84mol•L-1的稀硫酸480mL,回答下列问题:(1)需要98%密度为1.84g•cm-3的浓硫酸50mL
(2)配制时,必须使用的仪器有:烧杯、50mL量筒、500mL容量瓶、玻璃棒,还缺少的仪器是胶头滴管.
(3)配制过程中用量筒量取浓硫酸时,俯视读数.对所配溶液浓度偏低(填“偏高”“偏低”“不影响”)
分析 配制480mL溶液,实际上配制的是500mL的溶液,
(1)先根据c=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度,再根据溶液稀释前后溶质的物质的量不变计算所需浓盐酸的体积;
(2)根据配制一定物质的量浓度的实验步骤选取实验仪器;
(3)分析不当操作对溶质的物质的量浓度和溶液的体积的影响,依据c=$\frac{n}{V}$进行误差分析.
解答 解:(1)浓硫酸的物质的量浓度为:c=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,设需要浓硫酸的体积为V,配制480mL溶液,实际上配制的是500mL的溶液,根据溶液稀释前后溶质的物质的量不变得:1.84mol/L×0.5L=18.4mol/L×V,解得:V=0.05L=50mL,
故答案为:50;
(2)配制步骤有量取、稀释、移液、洗涤、定容、摇匀等操作,一般用量筒量取浓硫酸在烧杯中稀释,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器还有胶头滴管,
故答案为:胶头滴管;
(3)用量筒量取浓硫酸时俯视刻度线,导致溶质的物质的量偏小,溶液的浓度偏低,
故答案为:偏低.
点评 考查一定物质的量浓度溶液的配制,题目难度不大,明确配制步骤为解答关键,误差分析为易错点,注意根据c=$\frac{n}{V}$分析溶液配制原理与误差分析,试题有利于提高学生的化学实验能力.

练习册系列答案
相关题目
1.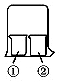 用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
 用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )| ①中的物质 | ②中的物质 | 预测①的现象 | |
| A | 酚酞溶液 | 浓盐酸 | 无明显变化 |
| B | 饱和的KNO3溶液 | 浓硫酸 | 无明显变化 |
| C | AlCl3溶液 | 浓氨水 | 有白色沉淀 |
| D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
| A. | A | B. | B | C. | C | D. | D |
11.下列溶液中的Cl-浓度与150mL、1mol•L-1MgCl2溶液中的Cl-浓度相等的是( )
| A. | 300 mL、1mol•L-1NaCl溶液 | B. | 75 mL、2mol•L-1CaCl2溶液 | ||
| C. | 150 mL、2mol•L-1KCl溶液 | D. | 75 mL、1mol•L-1AlCl3溶液 |
15.下列观点正确的是( )
| A. | 催化剂是影响化学反应速率的主要因素 | |
| B. | 化学反应的反应热与反应途径无关 | |
| C. | 增大压强一定能增大化学反应速率 | |
| D. | 反应物分子间发生碰撞即可发生化学反应 |
5.类推法在学习过程中经常应用.下列左边正确,类推法应用于右边也正确的是( )
| A | 向FeCl2溶液中滴入氯水2Fe2++Cl2═2Fe3++2Cl- | 向FeCl2溶液中滴入碘水2Fe2++I2═2Fe3++2I- |
| B | CO2通入漂白粉溶液中CO2+Ca2++2ClO-+H2O═CaCO3↓+2HClO | SO2通入漂白粉溶液中SO2+Ca2++2ClO-+H2O═CaSO3↓+2HClO |
| C | 向Na2CO3溶液中滴入稀HNO3CO32-+2H+═CO2↑+H2O | 向Na2SO3溶液中滴入稀HNO3SO32-+2H+═SO2↑+H2O |
| D | 向澄清石灰水中通入少量CO2 气体Ca2++2OH-+CO2═CaCO3↓+H2O | 向澄清石灰水中通入少量SO2 气体Ca2++2OH-+SO2═CaSO3↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
12.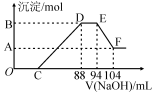 实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.现有一定量铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入2mol.L-l的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.现有一定量铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入2mol.L-l的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )
 实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.现有一定量铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入2mol.L-l的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.现有一定量铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入2mol.L-l的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )| A. | 反应前的溶液中,硝酸的物质的量为0.2 mol | |
| B. | C点对应NaOH溶液的体积为48 mL | |
| C. | 样品中铝粉和铁粉的物质的量之比为5:3 | |
| D. | D点与A点沉淀物质的量的差为0.02 mol |
9.一定能在下列溶液中大量共存的离子组是( )
| A. | 水电离产生的H+浓度为1×10-12mol•L-1的溶液:NH4+、Na+、Cl-、CO32- | |
| B. | 能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32- | |
| C. | 0.1 mol/L的NaNO3溶液中:H+、Fe2+、Cl-、SO42- | |
| D. | 含有大量Al3+的水溶液中:Na+、NH4+、HCO3-、Br- |
10.在酸性溶液中能大量共存而且为无色透明的溶液是( )
| A. | NH4+、Al3+、SO42-、NO3- | B. | K+、Fe2+、NO3-、SO42- | ||
| C. | K+、MnO4-、NH4+、NO3- | D. | Na+、K+、ClO-、NO3- |